等效平衡(1)等效平衡问题可以用“三个两”来概括或帮助我们记忆,即:“两种反应”(反应前后气体分子数可变的反应和反应前后气体分子数不变的反应),“两种条件”(恒温恒容和恒温恒压),“两种等效”(投料相同和投料比相同)
(2)根据反应条件(恒温恒压或恒温恒容)以及可逆反应的特点(反应前后气体分子数是否相等),可将等效平衡问题分成三类:①恒温、恒容条件下,反应前后气体分子数不相等的可逆反应:只要改变起始加入物质的物质的量,若通过可逆反应的化学计量数换算成同一半边的物质的物质的量,若与原平衡相同,则两平衡等效(即投料相同,此法又称一边倒法)
举例:2A(g)+B(g)3C(g)+D(g)ABCD等效说明①2mol1mol00①③⑤互为等效平衡,表现在物质的量、质量、体积、物质的量浓度、组分百分含量(摩尔分数、质量分数、体积分数)相同②4mol2mol00③1mol0
5mol④01mol3mol1mol⑤003mol1mol②恒温、恒容条件下,反应前后气体分子数相等的可逆反应:只要换算到同一半边时,反应物(或生成物)的物质的量的比例与原平衡相等,则两平衡等效(即投料比相同)
举例:2A(g)+B(g)3C(g)+D(s)ABCD等效说明①2mol1mol00①②③⑤互为等效平衡,表现在组分百分含量(摩尔分数、质量分数、体积分数)相同②4mol2mol00③1mol0
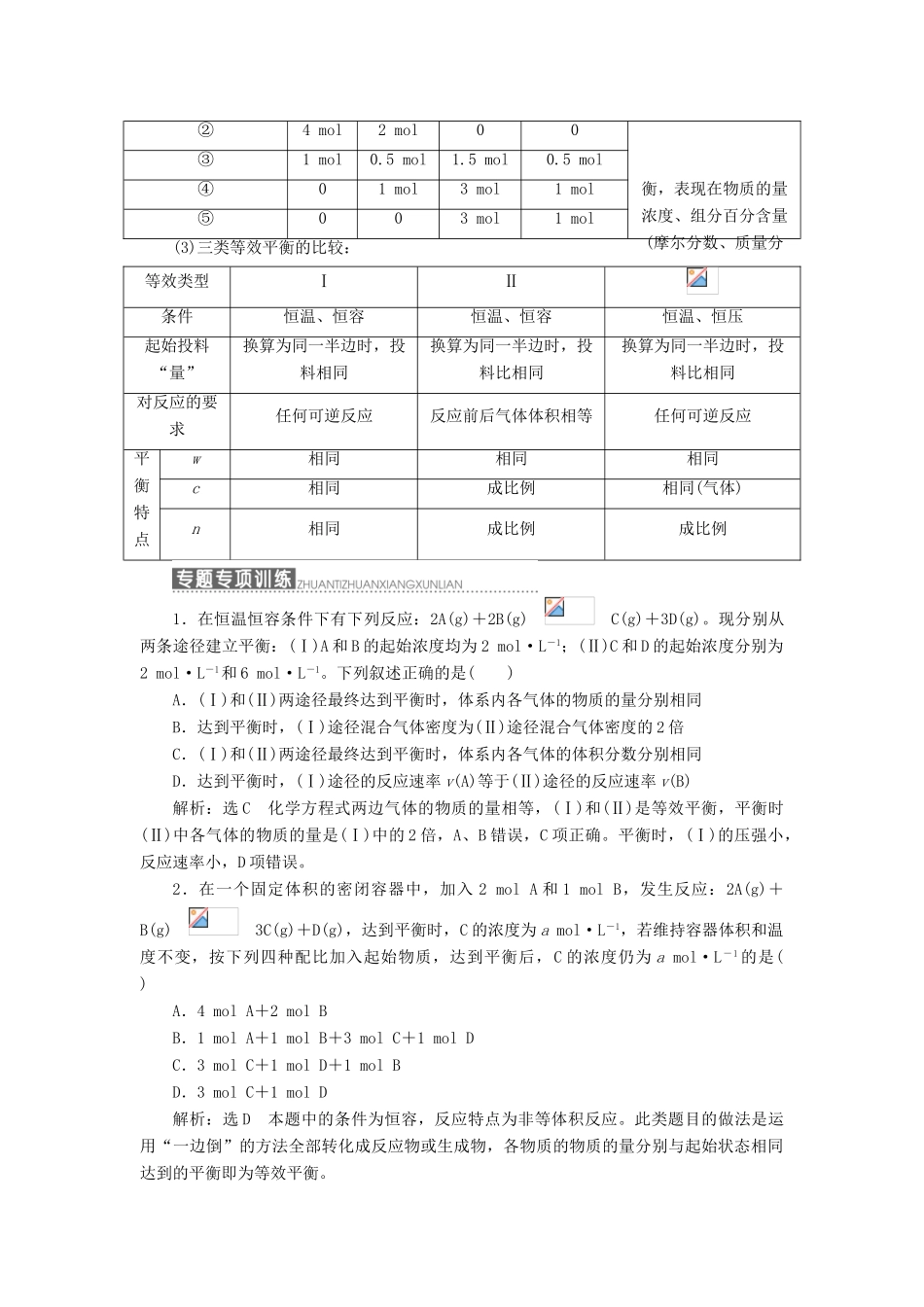
5mol④01mol3mol1mol⑤003mol1mol③恒温、恒压条件下,反应前后气体分子数任意型的可逆反应:只要按化学计量数换算到同一半边后,各物质的物质的量之比与原平衡相等,则两平衡等效(即投料比相同)
举例:2A(g)+B(g)3C(g)+D(g)ABCD等效说明①②③⑤互为等效平①2mol1mol00衡,表现在物质的量浓度、组分百分含量(摩尔分数