弱电解质的电离平衡1.化学平衡状态的特征有哪些
提示:(1)动态平衡;(2)达到平衡时,正、逆反应速率相等;(3)平衡时,各物质的浓度保持不变;当条件改变时,平衡被破坏,可能发生移动
2.化学平衡移动原理的内容是什么
提示:改变影响化学平衡的一个因素,平衡将向着能够减弱这种改变的方向移动
3.影响化学平衡常数的因素是什么
4.强、弱电解质的电离差异是什么
提示:强电解质在水溶液中完全电离,弱电解质在水溶液中部分电离
[新知探究]探究1弱电解质电离平衡的建立(1)弱电解质电离平衡的建立图示:(2)电离平衡概念:在一定条件(如温度、浓度一定)下,当弱电解质在水溶液中电离达到最大程度时,电离过程并没有停止,此时弱电解质电离成离子的速率和离子结合成弱电解质分子的速率相等,溶液中各分子和离子的浓度都不再发生变化,就达到了电离平衡
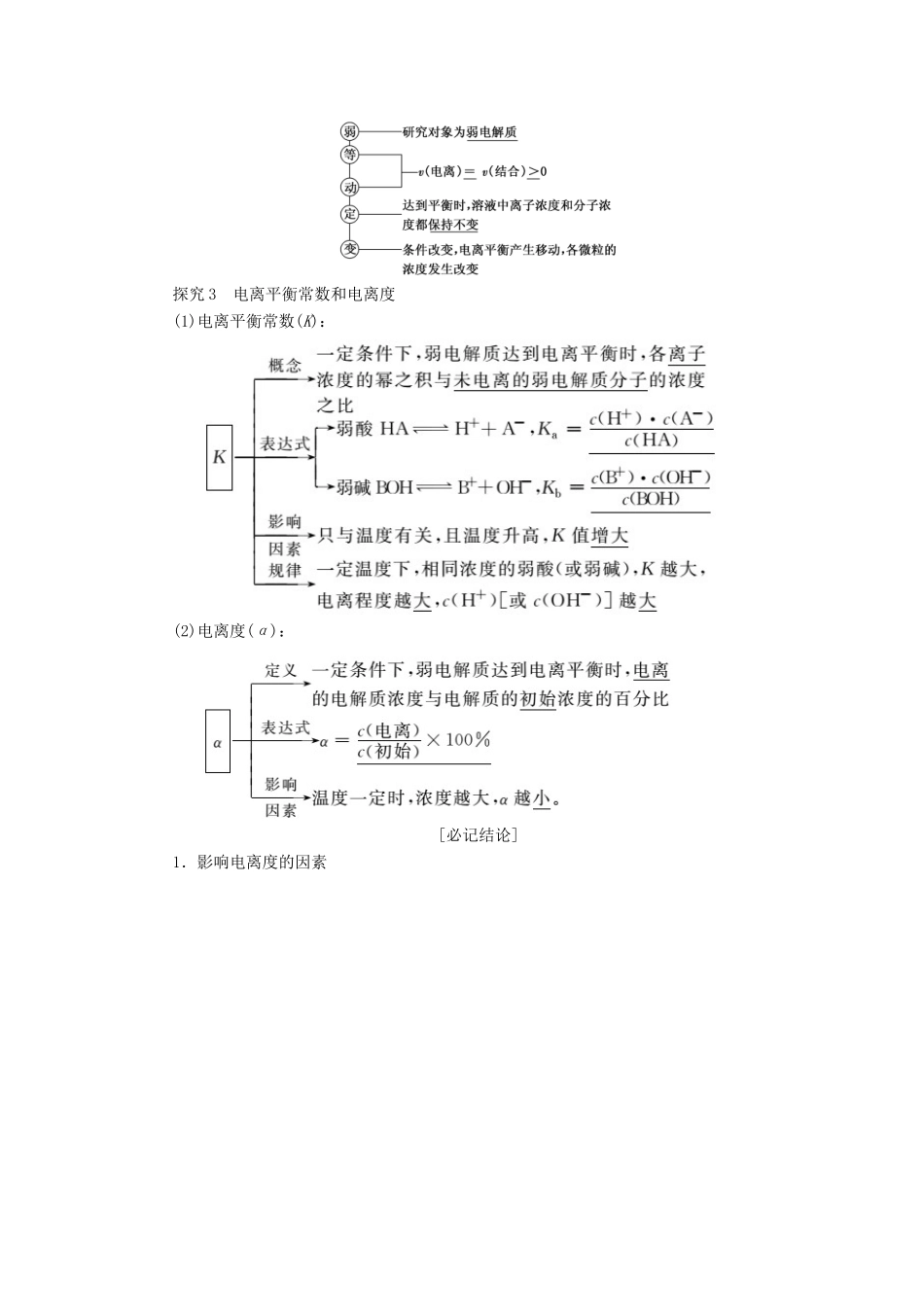
探究2电离平衡的特征探究3电离平衡常数和电离度(1)电离平衡常数(K):(2)电离度(α):[必记结论]1.影响电离度的因素2
影响电离平衡的因素以0
1mol·L-1的CH3COOH为例(CH3COOHH++CH3COO-),当改变条件,其平衡移动方向、Ka、n(H+)、导电性变化如下表:[成功体验]1.在含有酚酞的0
1mol·L-1氨水中加入少量的NH4Cl晶体,则溶液的颜色()A.变蓝色B.变深C.变浅D.不变解析:选CNH3·H2O是弱电解质,在溶液中存在电离平衡:NH3·H2ONH+OH-,当加入NH4Cl晶体时,c(NH)增大,使上述平衡向逆反应方向移动,c(OH-)减小,溶液颜色变浅
2.(好题共享·选自人教版教材P44·T4)已知25℃下,醋酸溶液中存在下述关系:=1
75×10-5其中的数值是该温度下醋酸的电离平衡常数
试回答下述问题:(1)当向该溶液中加入一定量的盐酸时,上式中的数值是否发生变化
(2)若醋酸