盐类水解课题名称盐类水解(复习课)教学目标1、知识与技能1、理解盐类水解的本质和盐类水解对溶液酸碱性的影响及变化规律
2、会写盐类水解的离子方程式与化学方程式
3、让学生了解盐类水解原理的应用
2、过程与方法创设问题情景,引导学生提出问题,培养学生质疑能力
运用实验验证质疑,并应用定量的方式解决学生常出现的疑惑,作为解决问题的新手段
3、情感、态度与价值观通过问题导学和针对性练习的训练,让学生体会复习过程的系统、严密与循序渐进
教学重点难点重点:1、盐类水解的原理2、实验设计盐类水解平衡移动的事实3、盐类水解定量的运算难点:影响水解平衡的因素和水解应用的关系教学准备药品仪器:三瓶失去标签NaCl溶液、Al2(SO4)3溶液、Na2CO3溶液,PH试纸,标准比色卡,表面皿,玻璃棒,烧杯,滤纸,酚酞溶液,BaCl2溶液PPT课件教学进程教师活动学生活动设计意图课堂引入问题探究1
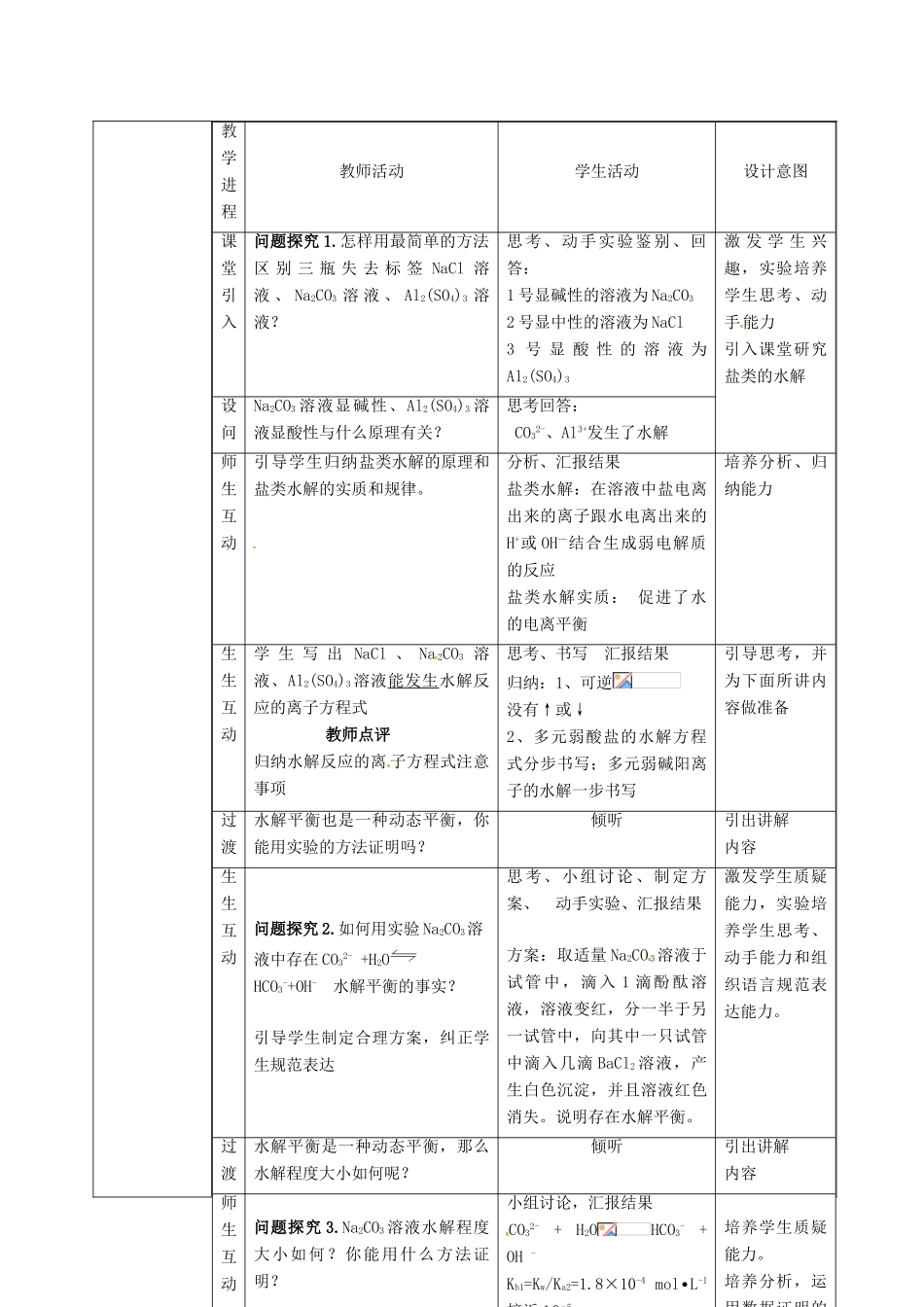
怎样用最简单的方法区别三瓶失去标签NaCl溶液、Na2CO3溶液、Al2(SO4)3溶液
思考、动手实验鉴别、回答:1号显碱性的溶液为Na2CO32号显中性的溶液为NaCl3号显酸性的溶液为Al2(SO4)3激发学生兴趣,实验培养学生思考、动手能力引入课堂研究盐类的水解设问Na2CO3溶液显碱性、Al2(SO4)3溶液显酸性与什么原理有关
思考回答:CO32-、Al3+发生了水解师生互动引导学生归纳盐类水解的原理和盐类水解的实质和规律
分析、汇报结果盐类水解:在溶液中盐电离出来的离子跟水电离出来的H+或OH—结合生成弱电解质的反应盐类水解实质:促进了水的电离平衡培养分析、归纳能力生生互动学生写出NaCl、Na2CO3溶液、Al2(SO4)3溶液能发生水解反应的离子方程式教师点评归纳水解反应的离子方程式注意事项思考、书写汇报结果归纳:1、可逆没有↑或↓2、多元弱酸盐的水解方程式分步书写;多元弱碱阳离子的水