第一单元化学反应中的热效应第三课时反应热的计算一、教学目标1、深刻理解基本概念,如反应热、焓变、燃烧热、盖斯定律等
2、根据热化学方程式进行有关的计算二、教学重点、难点1、盖斯定律在计算中的应用三、教学方法:讲授法四、教学过程【复习提问】1、什么是热化学方程式
书写热化学方程式要注意哪些要点
2、写出下列反应的热化学方程式(1)1molC2H5OH(l)与适量O2(g)反应,生成CO2(g)和H2O(l),放出1366
(2)18g葡萄糖与适量O2(g)反应,生成CO2(g)和H2O(l),放出280
【讲解】化学反应的反应热,有的能够测量,有的不能测量
比如将一些生成不稳定物质的化学反应,例有CCO,CO或多或少的要转化为CO2,还有一些反应进行的比较慢,要几天,几个月,几年,甚至几十年,肯定不能测量
对于这样的反应热,我们就要进行计算才能得到
这节课我们就来讲讲反应焓变的计算
【板书】一、反应焓变的计算【讲解】反应焓变之所以能够有计算得出,要归功于瑞士科学家盖斯提出的盖斯定律,我们来看看该定律的内容
【板书】(一)盖斯定律:1、内容:对于一个化学反应,无论是一步完成还是分几步完成,其反应焓变都是一样的
【讲解】这就说明对于化学反应,只要其反应物和反应产物确定了,不管它中间经历了多少步,反应焓变总是一定的
好比一个人登山,不管他选择什么途径,只要他从山脚到了山顶,他攀爬的高度总是一定的
这也说明了反应焓变有点像物理学中的矢量
究其原因是焓是一个状态函数
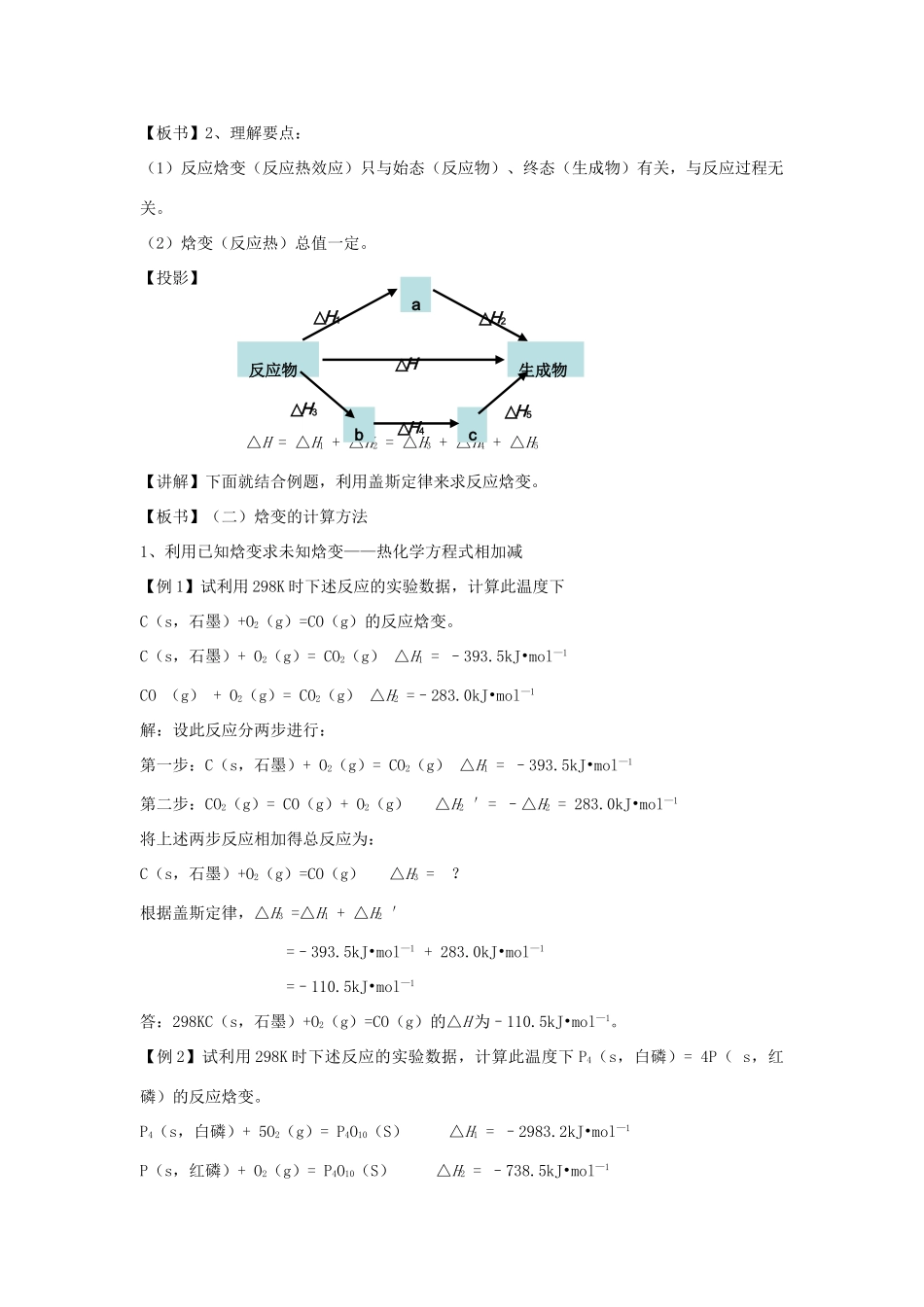
【板书】2、理解要点:(1)反应焓变(反应热效应)只与始态(反应物)、终态(生成物)有关,与反应过程无关
(2)焓变(反应热)总值一定
【投影】△H=△H1+△H2=△H3+△H4+△H5【讲解】下面就结合例题,利用盖斯定律来求反应焓变
【板书】(二)焓变的计算方法1、利用已知焓变求未知焓变——