第四单元电解原理及其应用第一节电解原理重点难点:1.理解电解的基本概念和原理
2.了解铜的电解精炼、电镀铜
3.会写电极反应式、电解方程式,掌握围绕电解的计算
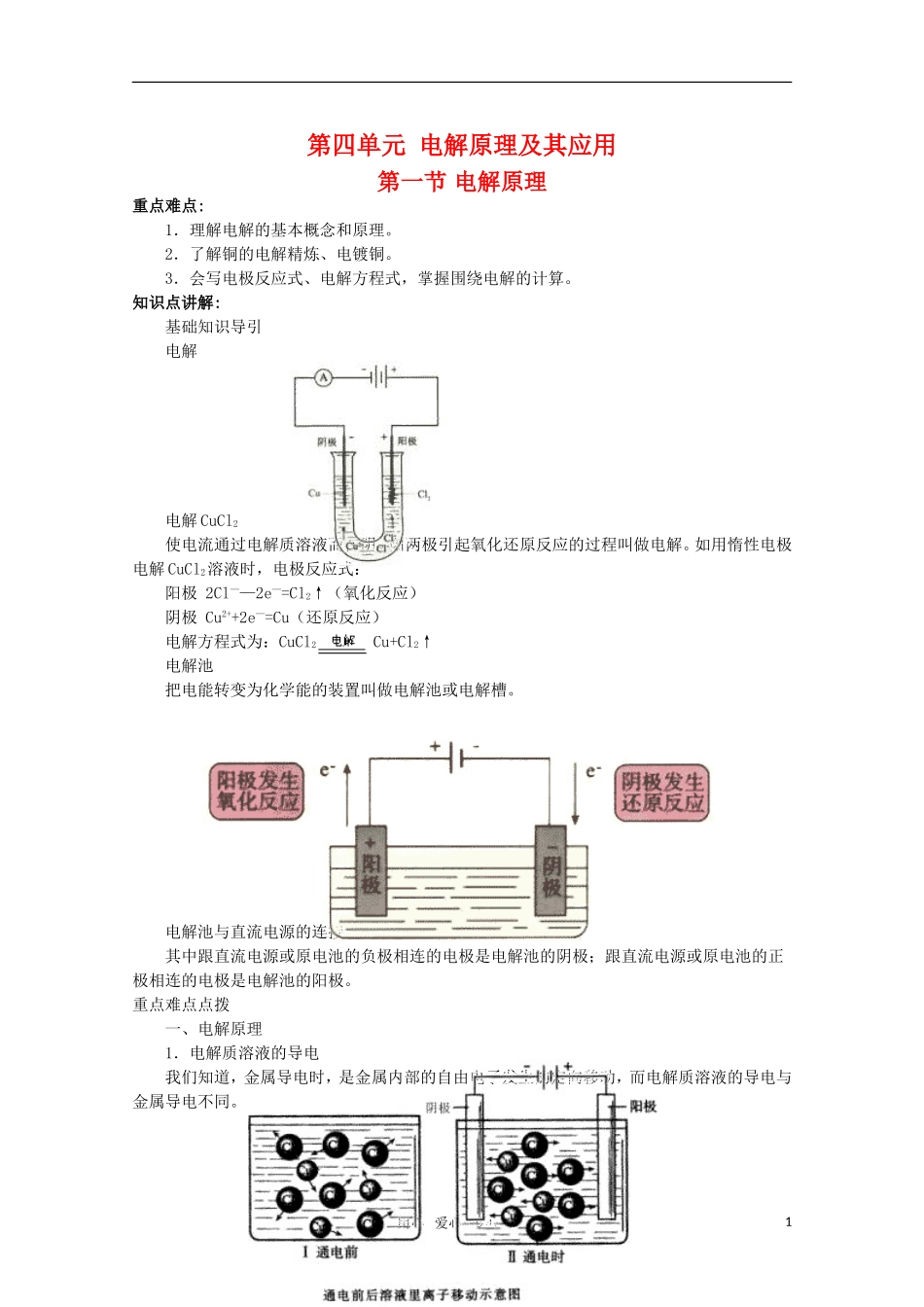
知识点讲解:基础知识导引电解电解CuCl2使电流通过电解质溶液而在阴、阳两极引起氧化还原反应的过程叫做电解
如用惰性电极电解CuCl2溶液时,电极反应式:阳极2Cl——2e—=Cl2↑(氧化反应)阴极Cu2++2e—=Cu(还原反应)电解方程式为:CuCl2Cu+Cl2↑电解池把电能转变为化学能的装置叫做电解池或电解槽
电解池与直流电源的连接其中跟直流电源或原电池的负极相连的电极是电解池的阴极;跟直流电源或原电池的正极相连的电极是电解池的阳极
重点难点点拨一、电解原理1.电解质溶液的导电我们知道,金属导电时,是金属内部的自由电子发生的定向移动,而电解质溶液的导电与金属导电不同
用心爱心专心1通电前电解质溶液中阴、阳离子在溶液中自由地移动;通电后在电场的作用下,这些自由移动的离子改作定向移动,带负电荷的阴离子由于静电作用向阳极移动,带正电荷的阳离子则向阴极移动,并在两极上发生氧化还原反应
我们把:借助于电流引起氧化还原反应的装置,也就是把电能转化为化学能的装置叫电解池
电解池中与直流电源负极相连的电极叫阴极,与直流电源正极相连的电极叫阳极
物质能否导电是由其内部能否形成定向移动的自由电荷所决定的,对金属就是自由电子,而对电解质溶液就是自由移动的阴阳离子
2.电解(1)概念:使电流流过电解质溶液而在阴、阳两极引起氧化还原反应的过程叫电解
(2)电子流动的方向:电子从外接直流电源的负极流出,经导线到达电解池的阴极,电解池溶液中的阳离子移向阴极,并在阴极获得电子而被还原,发生还原反应;与此同时,电解池溶液中的阴离子移向阳极,并在阳极上失去电子(也可能是阳极很活泼而本身失去电子)而被氧化,发生氧化反应
这样,电子又从电解池的阳