第三单元金属的腐蚀与防护教案7(1-3-1:金属的腐蚀与防护)教学目标:1.了解什么是金属的腐蚀,金属腐蚀的本质是什么
2.了解一般金属的腐蚀可分为哪几种
3.了解一般金属的防护方法
教学重点:钢铁的吸氧腐蚀及防护发方法
教学难点:金属腐蚀的本质
教学模式:自学探究讲练结合教学过程:一、自学探究1.什么是金属的腐蚀
金属腐蚀的本质是什么
3.由于金属接触的介质不同,一般金属的腐蚀可分为几种
4.什么是化学腐蚀
5.什么是电化学腐蚀
6.在潮湿的空气里,钢铁制品的表面为什么会形成无数微小的原电池
吸氧腐蚀:条件负极:正极:析氢腐蚀:条件负极:正极:二.总结(一)、金属的电化学腐蚀1.金属腐蚀:金属(或合金)跟周围接触到的气体(或液体)反应而腐蚀损耗的过程
2.金属腐蚀的本质:金属原子金属阳离子M-ne-=Mn+4.金属的化学腐蚀:金属跟接触到的物质直接发生化学反应而引起的腐蚀
特点:反应简单、金属与氧化剂之间的氧化还原反应
5.电化学腐蚀:不纯的金属或合金与电解质溶液接触,会发生原电池反应,比较活泼的金属失电子被氧化的腐蚀
1在这些微小的原电池里,做负极的铁失去电子被氧化,钢铁表面的水吸收氧气得电子生成OH-,这样钢铁制品被慢慢腐蚀
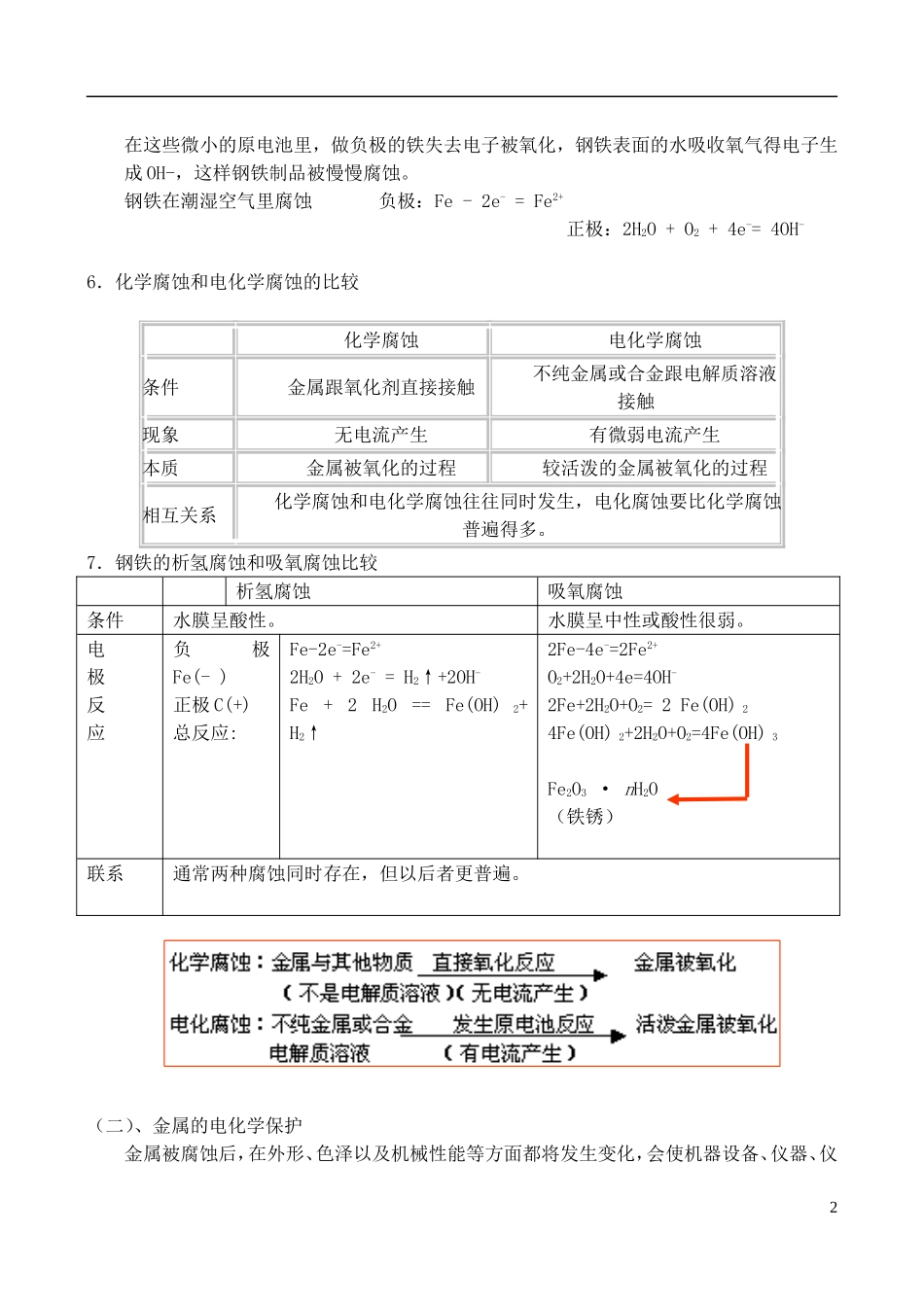
钢铁在潮湿空气里腐蚀负极:Fe-2e-=Fe2+正极:2H2O+O2+4e-=4OH-6.化学腐蚀和电化学腐蚀的比较化学腐蚀电化学腐蚀条件金属跟氧化剂直接接触不纯金属或合金跟电解质溶液接触现象无电流产生有微弱电流产生本质金属被氧化的过程较活泼的金属被氧化的过程相互关系化学腐蚀和电化学腐蚀往往同时发生,电化腐蚀要比化学腐蚀普遍得多
7.钢铁的析氢腐蚀和吸氧腐蚀比较析氢腐蚀吸氧腐蚀条件水膜呈酸性
水膜呈中性或酸性很弱
电极反应负极Fe(-)正极C(+)总反应:Fe-2e-=Fe2+2H2O+2e-=H2↑+2OH-F