第二节化学反应的限度【教学目标】了解化学平衡的概念和化学平衡状态的特征【教学重点】化学平衡的建立和特征【教学难点】化学平衡的建立【教学过程】〖引入〗化学反应有进行的快慢,有反应进行的程度,如N2+3H22NH3及溶解平衡
〖思考〗例举学过的有关可逆反应的例子
〖活动与探究〗教师、学生共同完成
实验证明许多反应都是可逆的
一、化学反应的限度化学反应:不可逆反应(相对的)和可逆反应
可逆反应:(1)同条件下、同时进行的反应(2)既可向正反应方向进行,又可以向逆反应方向进行
特点:可逆反应不能进行到底〖思考〗例举学过的有关可逆反应的例子
【拓展视野】高炉的尾气之谜
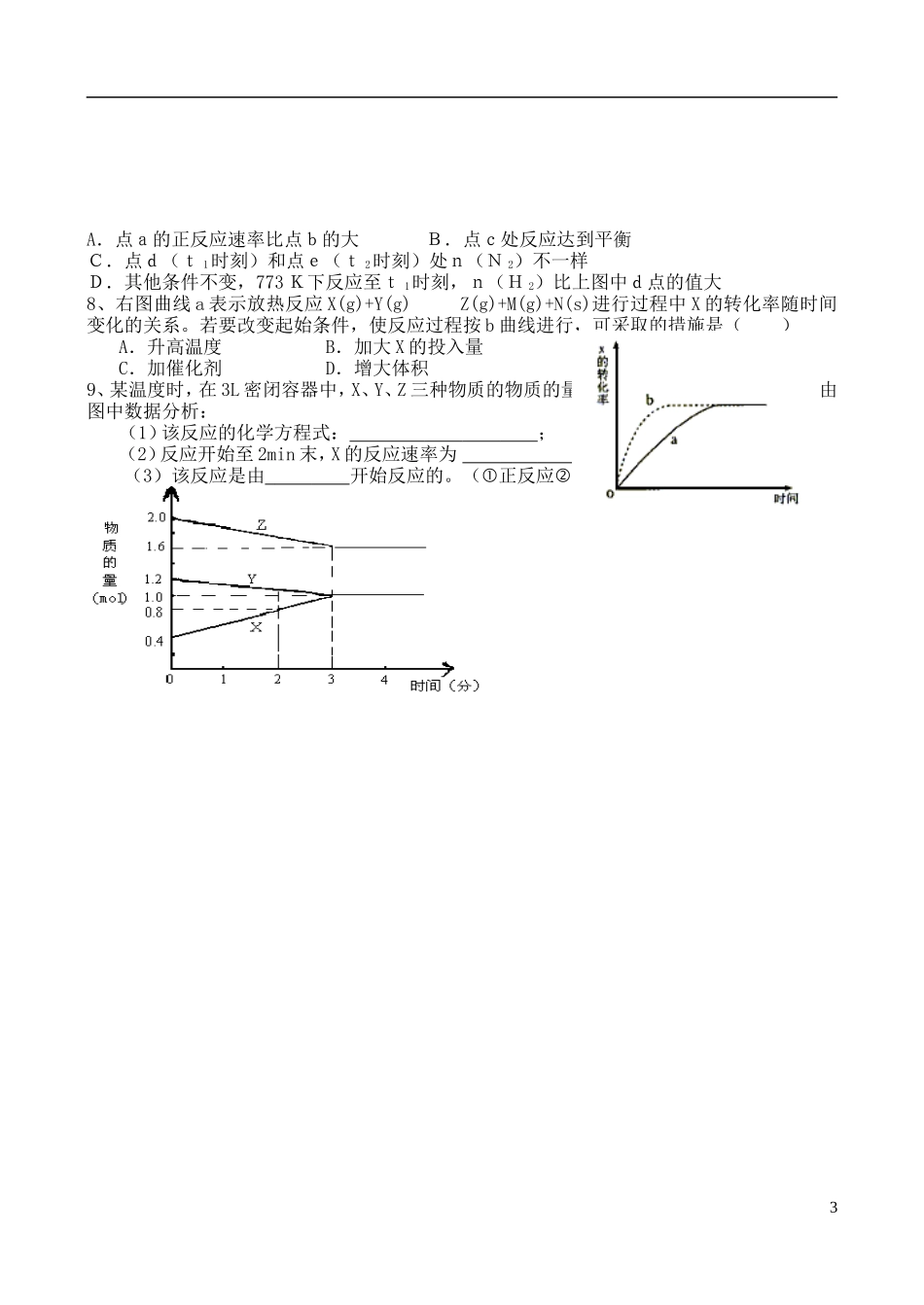
二、化学平衡1、研究对象:可逆反应2、化学平衡的图象表示法N2+3H22NH3〖思考〗1、反应刚开始时,反应物和生成物的浓度如何
正逆反应的速率如何
2、随反应的进行,反应物和生成物的浓度如何变化
正逆反应的速率如何
3、当正逆反应速率相等时,反应物和生成物的浓度如何变化
V-t图象:VV正V正=V逆V逆平衡状态t1t反应无论进行多长时间,反应后混合物中各种物质的浓度都不再发生变化(反应物和生成物共存于同一体系中)
3、化学平衡状态(1)化学平衡状态是可逆反应在一定条件下进行到一定程度时,正反应速率和逆反应速率相等,反应物和生成的浓度不再发生变化的状态
(2)化学平衡状态的特点:逆、等、动、定、变
①动:是指动态平衡
V(正)=V(逆)≠0②定:是指各组分的浓度保持不变
(物质的量、体积分数、压强、平均分子量)对于方程式两边体积相等的可逆反应,压强、平均分子量恒定时不一定是平衡状态
③变:是指外界条件改变,V(正)≠V(逆),化学平衡被破坏
(3)化学平衡状态的判断依据:V(正)=V(逆),反应物和生成的浓度不再发生变化
例题:能说明反应CO(g)+H2O(g)CO2(g)+H2(g)达到平衡的是A、容器内CO