第三节化学键(第1课时)三维目标知识与技能:1.掌握离子键的概念
2.掌握离子键的形成过程和形成条件,并能熟练地用电子式表示离子化合物的形成过程
过程与方法:1.通过对离子键形成过程的教学,培养学生抽象思维和综合概括能力;2.通过电子式的书写,培养学生的归纳比较能力,通过分子构型的教学培养学生的空间想像能力
情感、态度与价值观:1.培养学生用对立统一规律认识问题
2.培养学生怀疑、求实、创新的精神
教学重点:1.离子键和离子化合物的概念2.用电子式表示离子化合物的形成过程
教学难点:用电子式表示离子化合物的形成过程教具准备:多媒体课件、投影仪、盛有氯气的集气瓶、金属钠、小刀、滤纸、镊子、铁架台、石棉网、酒精灯、火柴
教学过程[新课导入]师:从前面所学知识我们知道,元素的化学性质主要决定于该元素的原子的结构
而化学反应的实质就是原子的重新组合,那么,是不是任意两个或多个原子相遇就都能形成新物质的分子或物质呢
板书:第三节化学键师:根据原子和原子相互作用的实质不同,我们可以把化学键分为离子键、共价键、金属键等不同的类型首先我们来学习离子键
板书:一、离子键[推进新课]师:要知道什么是离子键,还须从我们初中学过的离子化合物说起
什么是离子化合物
演示实验1—2:钠在氯气中燃烧
板书2Na+Cl2====2NaCl师:从宏观上看,钠和氯气发生了化学反应,生成了新物质氯化钠
如若从微观的角度,又应该怎样理解上述反应呢
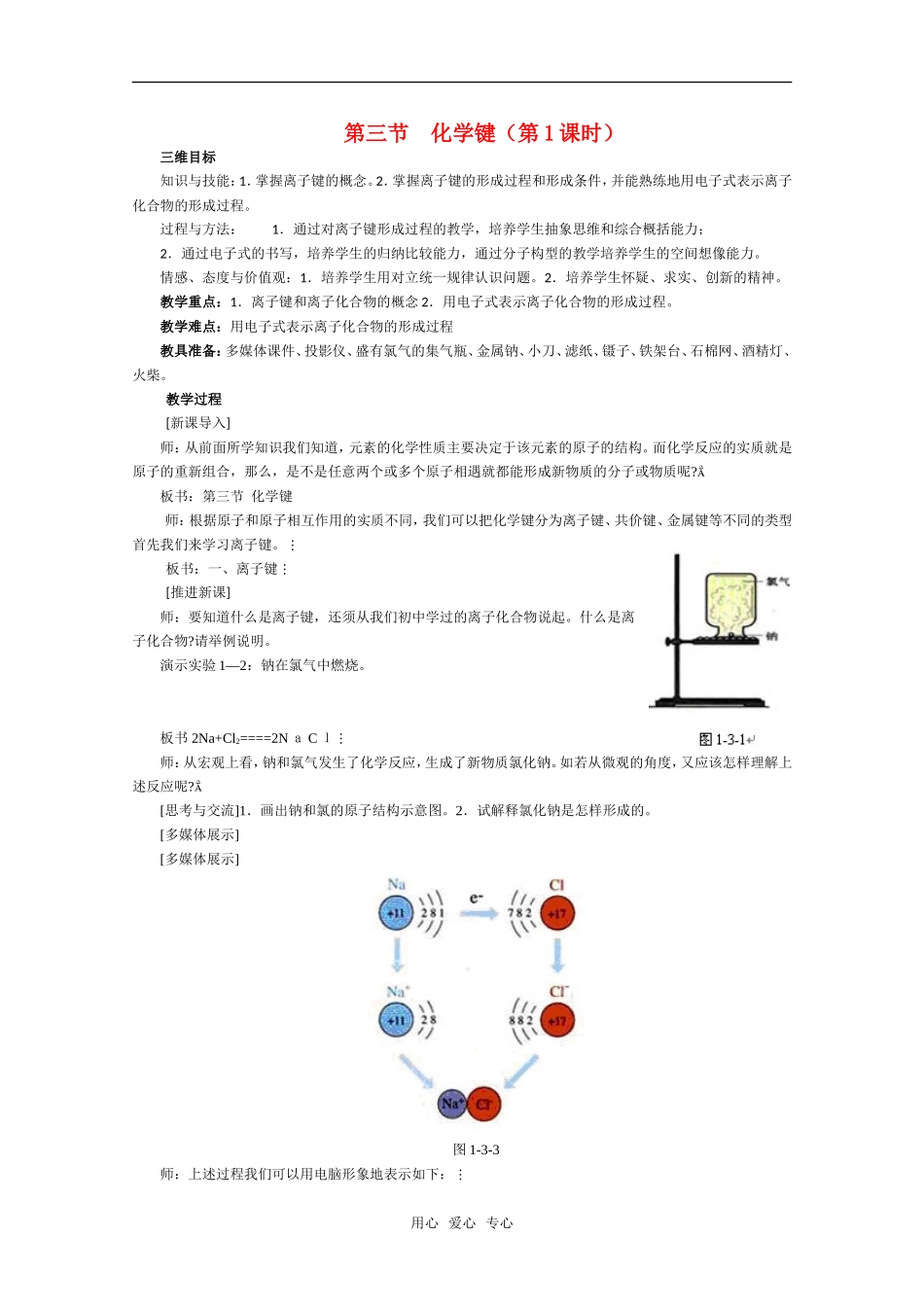
[思考与交流]1.画出钠和氯的原子结构示意图
2.试解释氯化钠是怎样形成的
[多媒体展示][多媒体展示]图1-3-3师:上述过程我们可以用电脑形象地表示如下:用心爱心专心[展示多媒体课件]①钠原子最外层1个电子在核外高速运动,氯原子最外层7个电子在核外高速运动;②钠原子与氯原子互相接近(发生反应);③钠原子最外层1个电子跑到氯原子上去