第2课时离子晶体[学习目标定位]1
正确理解离子键、离子晶体的概念,知道离子晶体类型与其性质的联系
认识晶格能的概念和意义,能根据晶格能的大小,分析晶体的性质
一离子晶体结构模型离子晶体中,阴离子呈等径圆球密堆积,阳离子有序地填在阴离子的空隙中,每个离子周围等距离地排列着异电性离子,被异电性离子包围
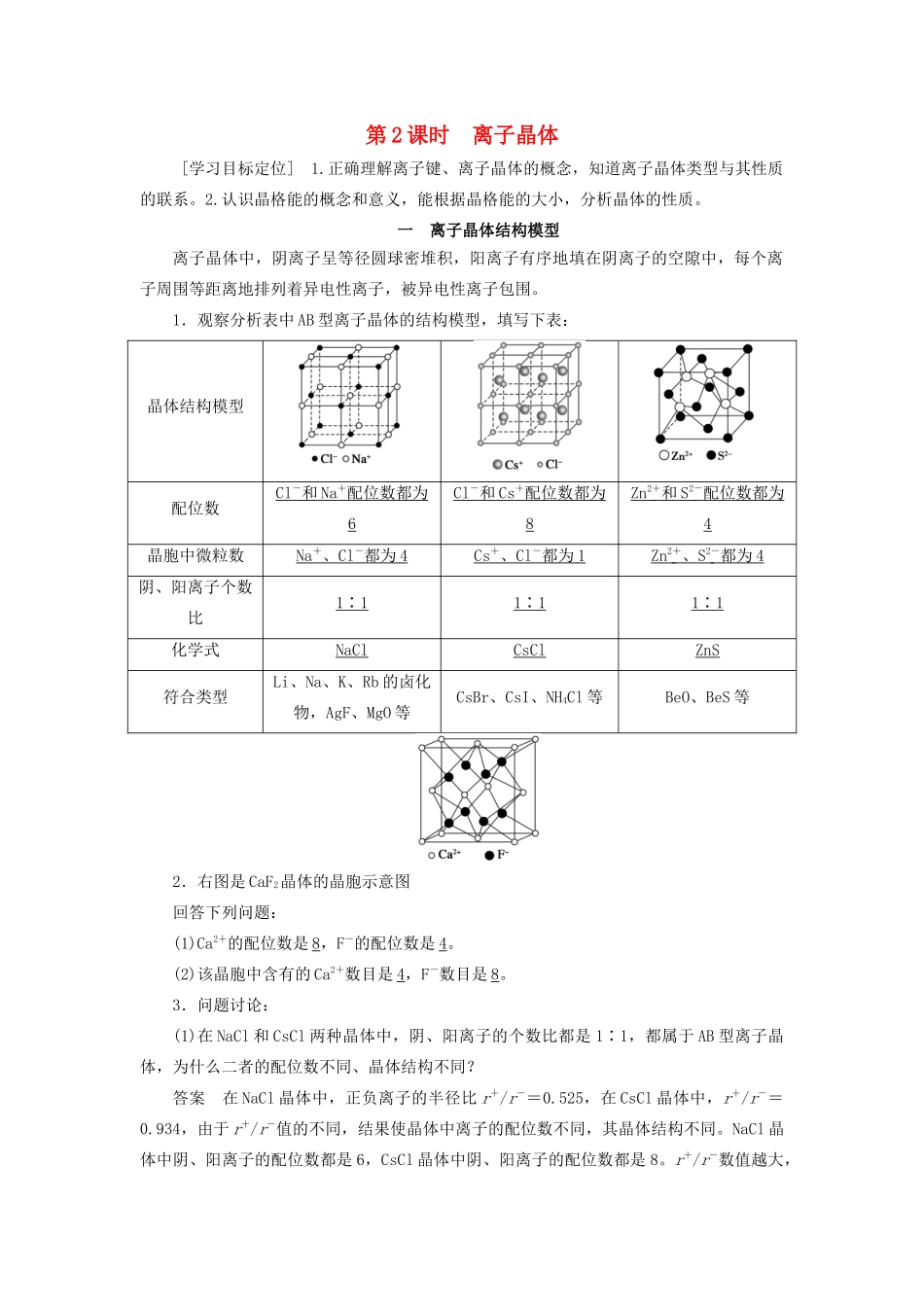
1.观察分析表中AB型离子晶体的结构模型,填写下表:晶体结构模型配位数Cl-和Na+配位数都为6Cl-和Cs+配位数都为8Zn2+和S2-配位数都为4晶胞中微粒数Na+、Cl-都为4Cs+、Cl-都为1Zn2+、S2-都为4阴、阳离子个数比1∶11∶11∶1化学式NaClCsClZnS符合类型Li、Na、K、Rb的卤化物,AgF、MgO等CsBr、CsI、NH4Cl等BeO、BeS等2.右图是CaF2晶体的晶胞示意图回答下列问题:(1)Ca2+的配位数是8,F-的配位数是4
(2)该晶胞中含有的Ca2+数目是4,F-数目是8
3.问题讨论:(1)在NaCl和CsCl两种晶体中,阴、阳离子的个数比都是1∶1,都属于AB型离子晶体,为什么二者的配位数不同、晶体结构不同
答案在NaCl晶体中,正负离子的半径比r+/r-=0
525,在CsCl晶体中,r+/r-=0
934,由于r+/r-值的不同,结果使晶体中离子的配位数不同,其晶体结构不同
NaCl晶体中阴、阳离子的配位数都是6,CsCl晶体中阴、阳离子的配位数都是8
r+/r-数值越大,离子的配位数越高
(2)为什么在NaCl(或CsCl)晶体中,正负离子的配位数相同;而在CaF2晶体中,正负离子的配位数不相同
答案在NaCl、CsCl晶体中,正负离子的配位数相同,是由于正负离子电荷(绝对值)相同,因而正负离子的个数相同,结果导致正负离子的配位数相同;若正负离子的电荷不相同,正负离子的个数必定不相同,结果正负离子的配位数就不会