第二节离子反应教案(第1课时)教学目标1
理解电解质的含义及强、弱电解质的区别;2
学习酸、碱、盐在水溶液中电离方程式的书写;3
从电离角度进一步认识酸、碱、盐
教学重点:电解质的判断、电离方程式的书写;教学难点:电解质的判断、电离方程式的书写;教学过程【引入】回顾化学反应的分类知识
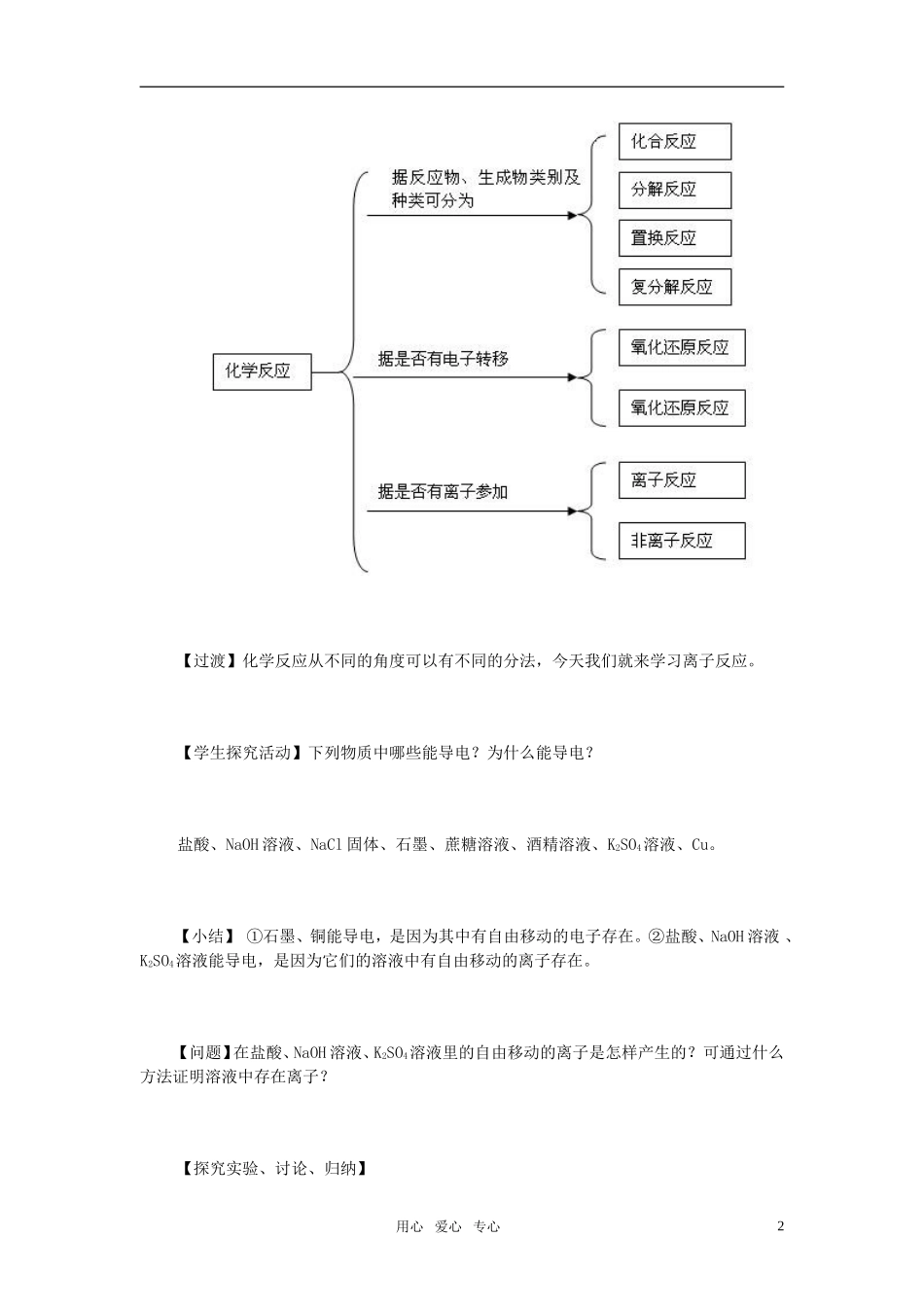
【学生探究活动活动】对所学过的化学反应进行分类
(由学生完成)用心爱心专心1【过渡】化学反应从不同的角度可以有不同的分法,今天我们就来学习离子反应
【学生探究活动】下列物质中哪些能导电
为什么能导电
盐酸、NaOH溶液、NaCl固体、石墨、蔗糖溶液、酒精溶液、K2SO4溶液、Cu
【小结】①石墨、铜能导电,是因为其中有自由移动的电子存在
②盐酸、NaOH溶液、K2SO4溶液能导电,是因为它们的溶液中有自由移动的离子存在
【问题】在盐酸、NaOH溶液、K2SO4溶液里的自由移动的离子是怎样产生的
可通过什么方法证明溶液中存在离子
【探究实验、讨论、归纳】用心爱心专心21、电离产生,其过程可用电离方程式来表示
2、可通过溶液导电性来检验
【板书】一、酸、碱、盐在水溶液中的电离【补充探究实验】盐酸、NaCl、NaCl水溶液、NaOH溶液、蔗糖溶液、酒精溶液、Cu等物质的导电情况
【板书】1、电解质电解质概念:课本P26在水溶液里或熔融状态下能够导电的化合物
如,酸、碱、盐等
【问题】相同条件下,不同类的酸、碱、盐溶液的导电能力是否相同
【学生探究实验、归纳总结】通过实验可知,相同条件下,不同类的酸、碱、盐溶液的导电能力不相同
电解质溶液导电能力的大小决定于溶液中自由移动的离子的浓度和离子所带的电荷数
而当溶液体积、浓度和离子所带的电荷数都相同的情况下,取决于溶液中自由移动离子数目,导电能力强的溶液里的自由移动的离子数目一定比导电能力弱的溶液里的自由移动的离子数目多
用心爱心专心3【板书】2、电解质的