4《等效平衡》教学设计化学平衡是历年来高考的重点和热点,而化学平衡中的“等效平衡”更是化学平衡中的难点,若能洞悉各类“等效平衡”的有关问题,那么一切有关化学平衡的问题也就迎刃而解了
“等效平衡”的问题已有较多的文章见诸报刊杂志,但在教学实践中教师和学生还是感到困难重重
如何突破这一难点,让学生不仅易于掌握,而且能灵活应用,就成为教学研究的一个重要课题
一、教学目标㈠知识与技能认识从不同起始状态下化学平衡的建立过程
㈡过程与方法通过典例分析,掌握分析等效平衡问题的方法
㈢情感态度价值观进一步培养学生自主合作探究的能力
二、教学重难点1
教学重点:等效平衡问题2
教学难点:应用勒夏特列原理分析各类等效平衡三、教学设计思路首先通过一些简单具体的例子,提出等效平衡的概念,然后应用勒夏特列原理分析各类等效平衡,从而理解各种类型等效平衡的模式,最后应用结论,分析复杂的问题
本教学案例的突出之处在于,应用勒夏特列原理分析等效平衡,让学生理解过程,从而能够深刻的理解应用,而不是简单的给出结论,让学生死记硬背,生搬硬套
如何设计合适的问题,引导学生得出结论,正是本教学设计试图解决的问题
教学过程设计【比喻】从我家到你家的中间有一个美丽的花园,从我家出发可以去,从你家出发也可以去,从我家和你家的任意一个地方出发都可以到达这个美丽的花园
引出课题:等效平衡问题
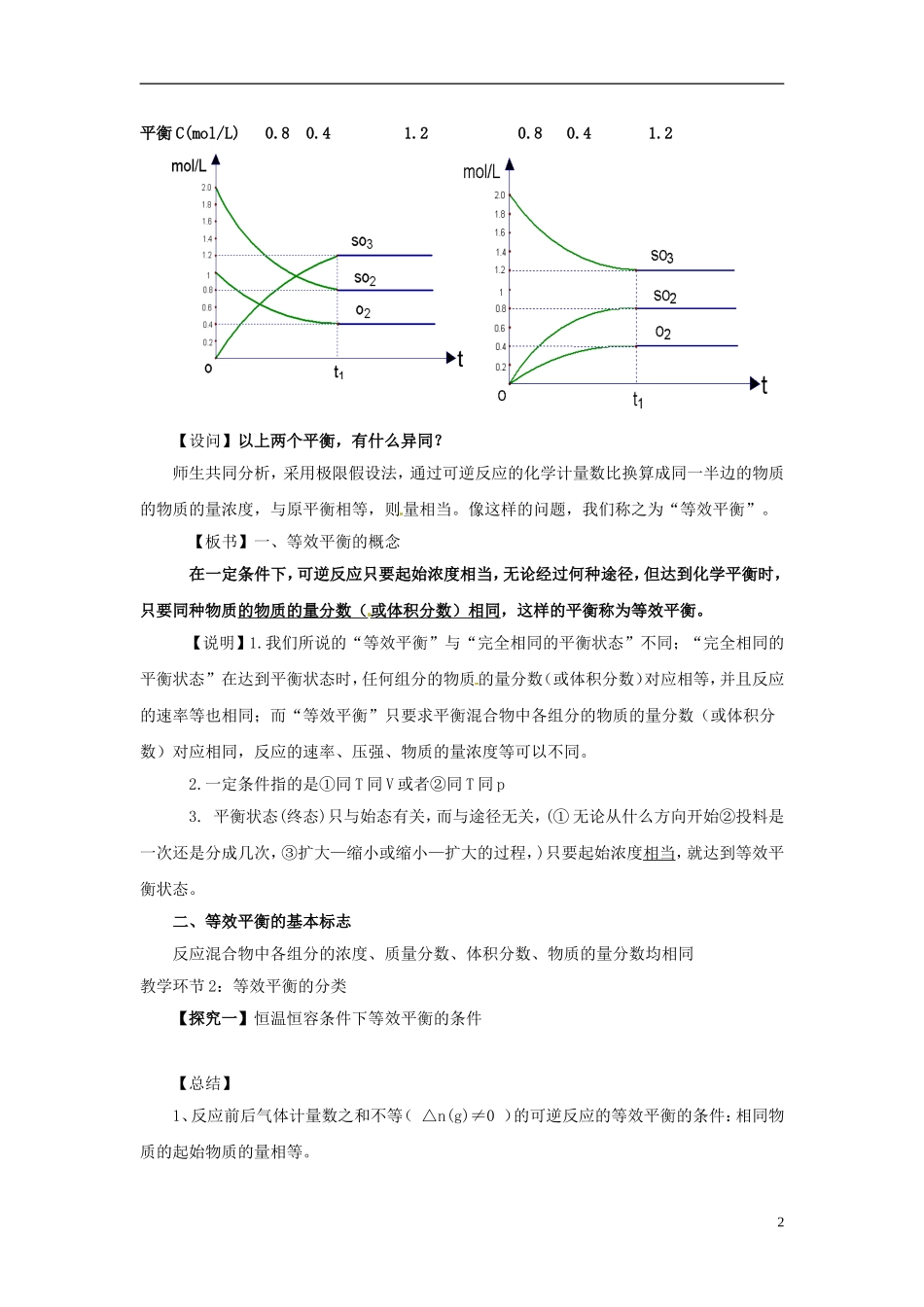
【例析】我们来看如下可逆反应,在一定条件下,按照不同的起始物质的量,达到平衡状态时,各种物质的物质的量分数之间有何关系:例:2SO2+O22SO3SO2+O22SO3起始C(mol/L)2100021平衡C(mol/L)0
2【设问】以上两个平衡,有什么异同
师生共同分析,采用极限假设法,通过可逆反应的化学计量数比换算成同一半边的物质的物质的量浓度,与原平衡相等,则量相当
像这样的问题,我们称之为“等