第十八单元化学定量实验复习要求掌握物质的量浓度溶液的配制、硫酸铜晶体中结晶水含量的测定,中和滴定的实验原理、操作方法,中和热的测定,以及盐的溶解度的测定,实验数据处理和误差分析方法等
一、配制一定物质的量浓度的溶液物质的量是化学上的重要物理量,是把宏观物质与微观粒子数联系起来的桥梁
物质的量浓度是以单位体积溶液里所含溶质的物质的量来表示溶液组成的物理量
实验仪器:烧杯、酸式滴定管、容量瓶(100mL)、胶头滴管、量筒、玻璃棒、药匙、滤纸、托盘天平
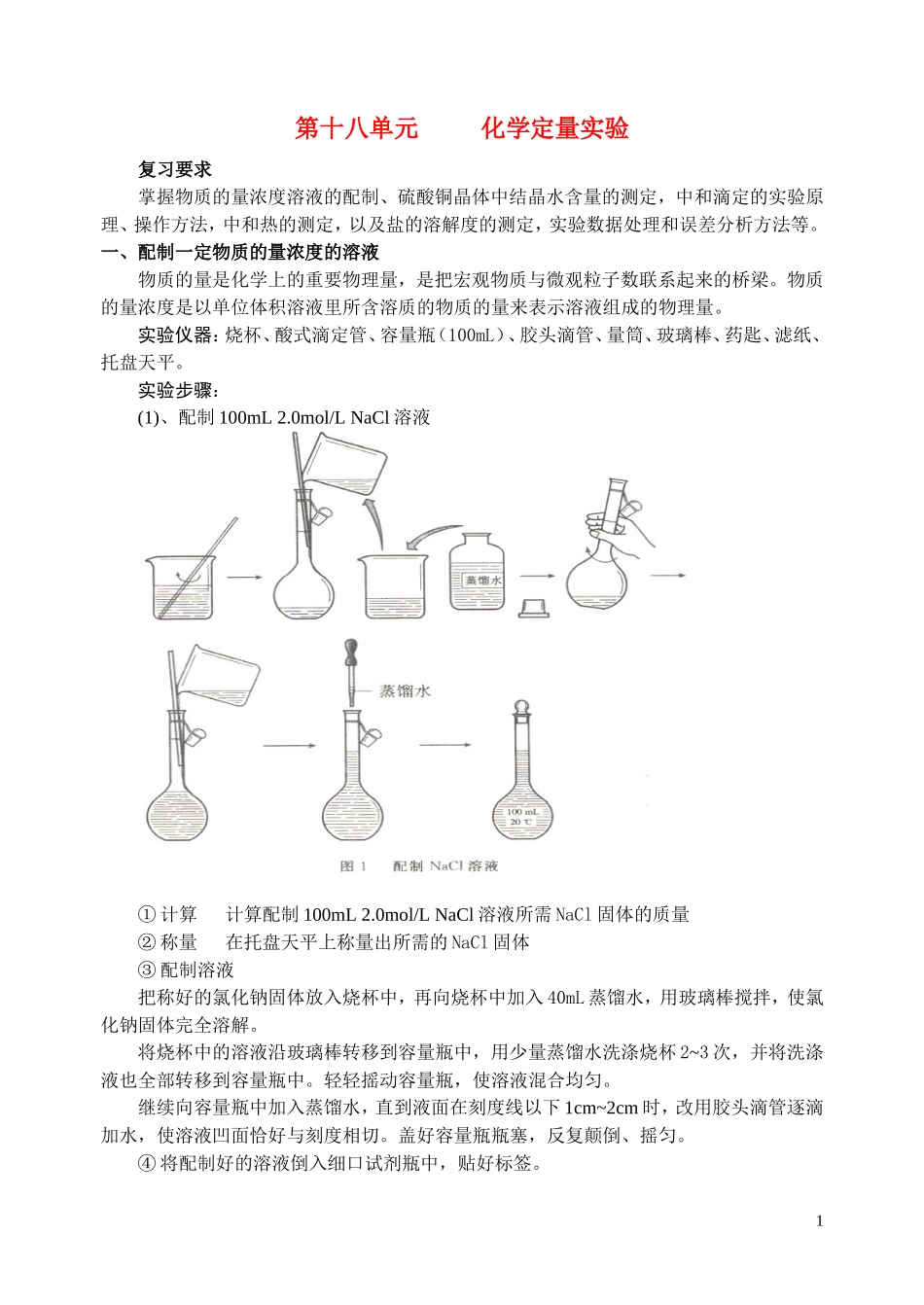
实验步骤:(1)、配制100mL2
0mol/LNaCl溶液①计算计算配制100mL2
0mol/LNaCl溶液所需NaCl固体的质量②称量在托盘天平上称量出所需的NaCl固体③配制溶液把称好的氯化钠固体放入烧杯中,再向烧杯中加入40mL蒸馏水,用玻璃棒搅拌,使氯化钠固体完全溶解
将烧杯中的溶液沿玻璃棒转移到容量瓶中,用少量蒸馏水洗涤烧杯2~3次,并将洗涤液也全部转移到容量瓶中
轻轻摇动容量瓶,使溶液混合均匀
继续向容量瓶中加入蒸馏水,直到液面在刻度线以下1cm~2cm时,改用胶头滴管逐滴加水,使溶液凹面恰好与刻度相切
盖好容量瓶瓶塞,反复颠倒、摇匀
④将配制好的溶液倒入细口试剂瓶中,贴好标签
1(2)用2
0mol/LNaCl溶液配制100mL0
5mol/LNaCl溶液①计算计算所需2
0mol/LNaCl溶液的体积②量取用酸式滴定管将所需体积的2
0mol/LNaCl溶液注入到烧杯中③配制溶液向盛有2
0mol/LNaCl溶液的烧杯中加入约20mL蒸馏水,用玻璃棒慢慢搅动,使其混合均匀
将烧杯中的溶液沿玻璃棒转移至容量瓶中
用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液也全部转移到容量瓶中,然后加水至刻度
盖好容量瓶瓶塞
反复颠倒、摇匀
④将配制好的100mL0
5mol/LNaCl溶液倒入指定的容器中
误差分析:下列操作