第1课时水的电离和溶液的酸碱性[明确学习目标]1
了解水的电离平衡及其影响因素
理解水的离子积常数
会计算溶液的pH
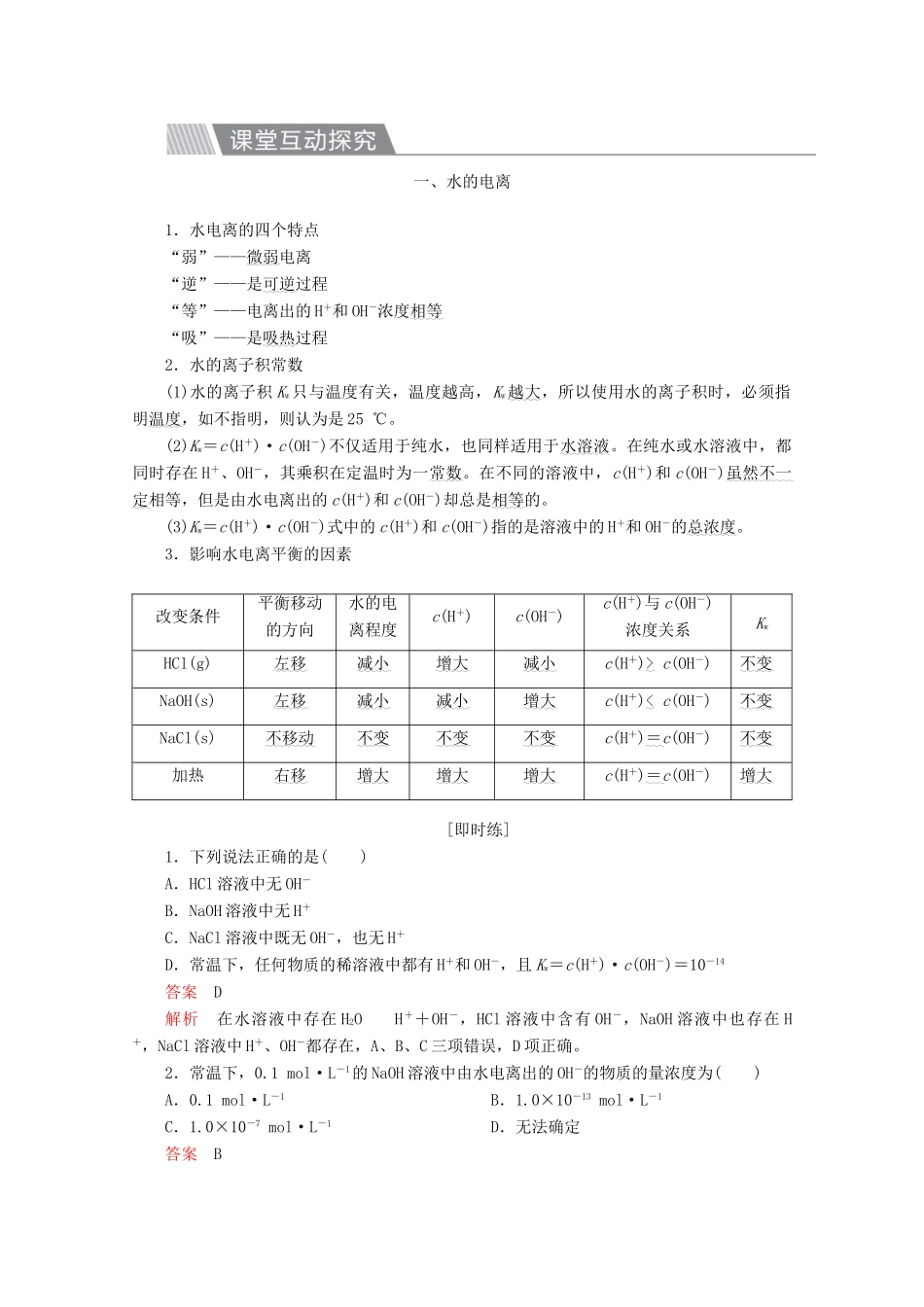
一、水的电离1.水的电离(1)水是一种极弱的电解质
(2)水的电离方程式为H2O+H2OH3O++OH-简写为□H2OH++OH-
(3)水的电离平衡常数K电离=
2.水的离子积常数(1)含义:因为水的浓度可看作常数,所以水中的□c(H+)·c(OH-)可看作常数,称为水的离子积常数,简称水的离子积,用Kw表示
(2)表达式与数值:表达式Kw=□c(H+)·c(OH-),室温时,Kw=□1
0×10-14
(3)影响因素:Kw只受□温度影响,由于水的电离是□吸热过程,温度升高,Kw□增大
二、溶液的酸碱性与pH1.溶液的酸碱性(1)溶液的酸碱性溶液酸碱性的判断标准是□c(H+)与c(OH-)相对大小
c(H+)□=c(OH-),溶液呈中性;c(H+)□>c(OH-),溶液呈酸性,且c(H+)越大,酸性□越强;c(H+)□<c(OH-),溶液呈碱性,且c(OH-)越大,碱性□越强
(2)溶液酸碱性的表示方法①当c(H+)或c(OH-)大于或等于1mol·L-1时,通常用□c(H+)或c(OH-)直接表示
②当c(H+)或c(OH-)小于1mol·L-1时,通常用□pH表示
2.溶液的pH(1)表达式:pH=□-lg_c(H+)
如c(H+)=1
0×10-5mol·L-1的酸性溶液,pH=5
(2)水溶液的pH、c(H+)及酸碱性的关系(25℃时)pH0≤pH