第二单元化学与资源开发利用课题二海水的综合利用第1课时教学目标1.了解氯碱工业反应原理;正确书写电极反应方程式和电解的总化学方程式
2.初步了解电解槽的简单结构及食盐水的精制
3.常识性介绍以氯碱工业为基础的化工生产
4.通过电解食盐水的实验,培养学生的观察能力、分析归纳能力和利用化学原理解决实际问题的能力
5.通过阅读材料,培养学生的自学能力
6.通过对实验现象的观察,掌握观察实验的方法和步骤,准确记录实验现象,正确分析实验现象,探究实验规律的方法
通过讨论,激发学生的求知欲,闪现智慧火花,培养创新意识
教学重点氯碱工业反应原理
教学难点氯碱工业反应原理
教学方法演示实验法教学用具1.实验仪器:铁架台、U型管、石墨电极、导线、电流表、直流电源
2.实验药品:饱和氯化钠溶液
3.幻灯片若干张
课时安排2课时引入新课:本节课我们学习电解饱和食盐水制烧碱——又称氯碱工业
我们学习的主要目标是掌握工业上制取氯气和烧碱的反应原理,初步了解化工生产设备、原料及其精制、生产流程
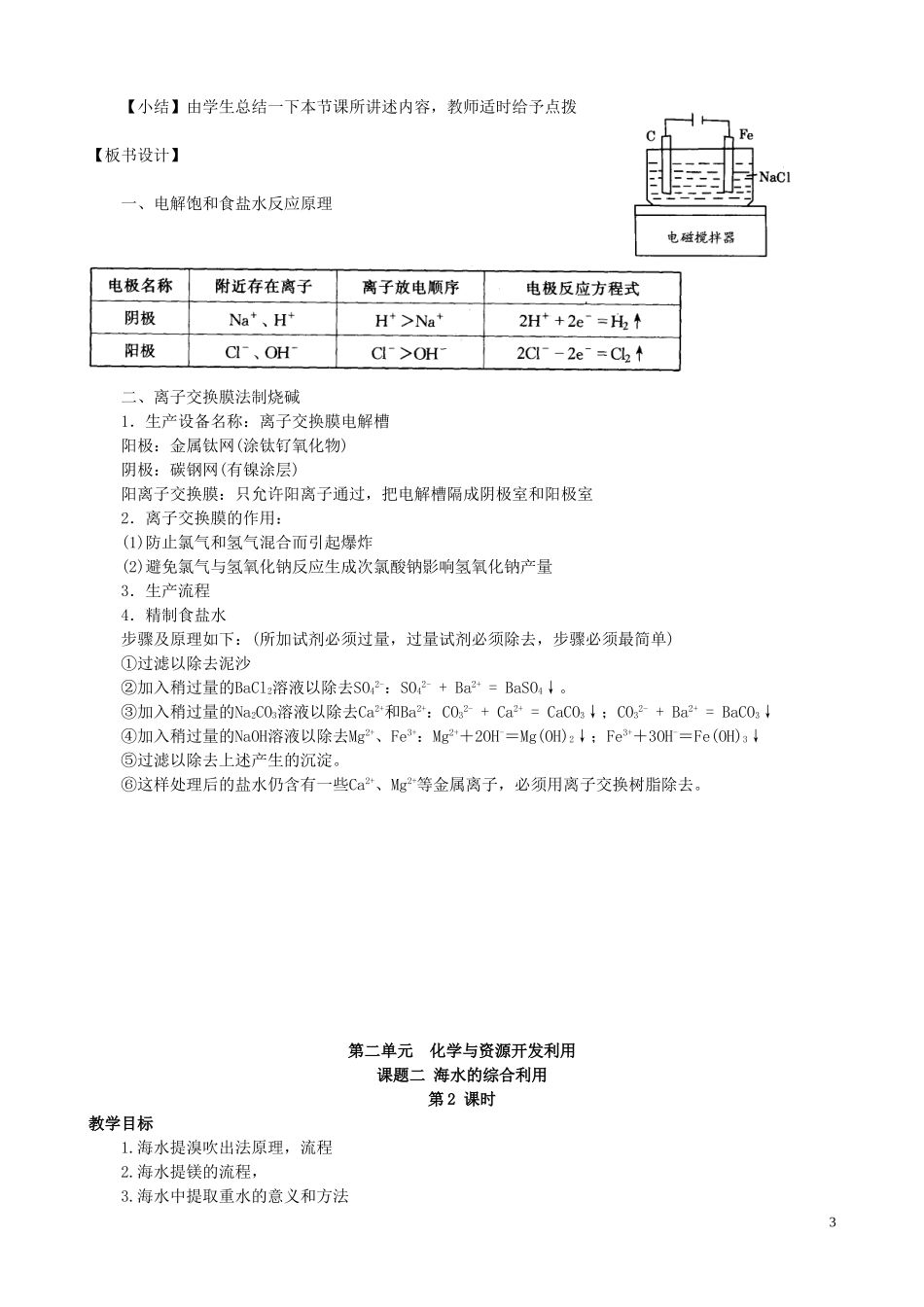
【板书】第二节氯碱工业一、电解饱和食盐水反应原理【演示】实验装置如右图:【投影】实验步骤:1.按装置图安装好仪器
2.向U型管中注人饱和食盐水,接通电源
3.向阴阳两极滴加几滴酚酞溶液,把湿润的淀粉碘化钾试纸分别放在阴阳两极试管口上方
【设疑】电解池两极上各有什么现象产生
【提问】请描述实验现象,试判断出结论
【学生回答】(相互补充)1.两极均产生气体
2.阴极区附近溶液出现红色,有碱生成
3.阳极淀粉碘化钾试纸变蓝,气体有刺激性气味,应是Cl2
【阅读讨论】阅读教材,看后相互讨论,推选代表回答产生这种现象的原因
【小结并板书】师生共同总结:在阴极:由于2H++2e-=H2↑,H+不断被消耗,促进H2OH++OH-向右移动,破坏了水的电离平衡,c(OH-)相对的增大了,因此,在阴极附近形成了氢氧化钠溶液