1《化学平衡与化学平衡常数》教学设计【教学目标】1、化学平衡常数的概念2、运用化学平衡常数对化学反应进行的程度判断3、运用化学平衡常数进行计算,转化率的计算【学习过程】【知识回顾】已知合成氨反应:N2(g)+3H2(g)2NH3(g)
在298K时:ΔH=-92
2kJ·mol-1ΔS=-198
2J·K-1·mol-1
请根据反应的焓变和熵变分析298K时合成氨反应能否自发进行
根据判据计算:ΔH-TΔS=-92
2kJ·mol-1-298K×(-198
2×10-3kJ·K-1·mol-1)=-33
1kJ·mol-1<0该反应常温下能自发进行,这是否就足够了呢
【新课引入】可逆反应进行到一定程度就会达到平衡状态,你知道这时平衡体系中反应物和生成物各占多少吗
反应到底进行到什么程度
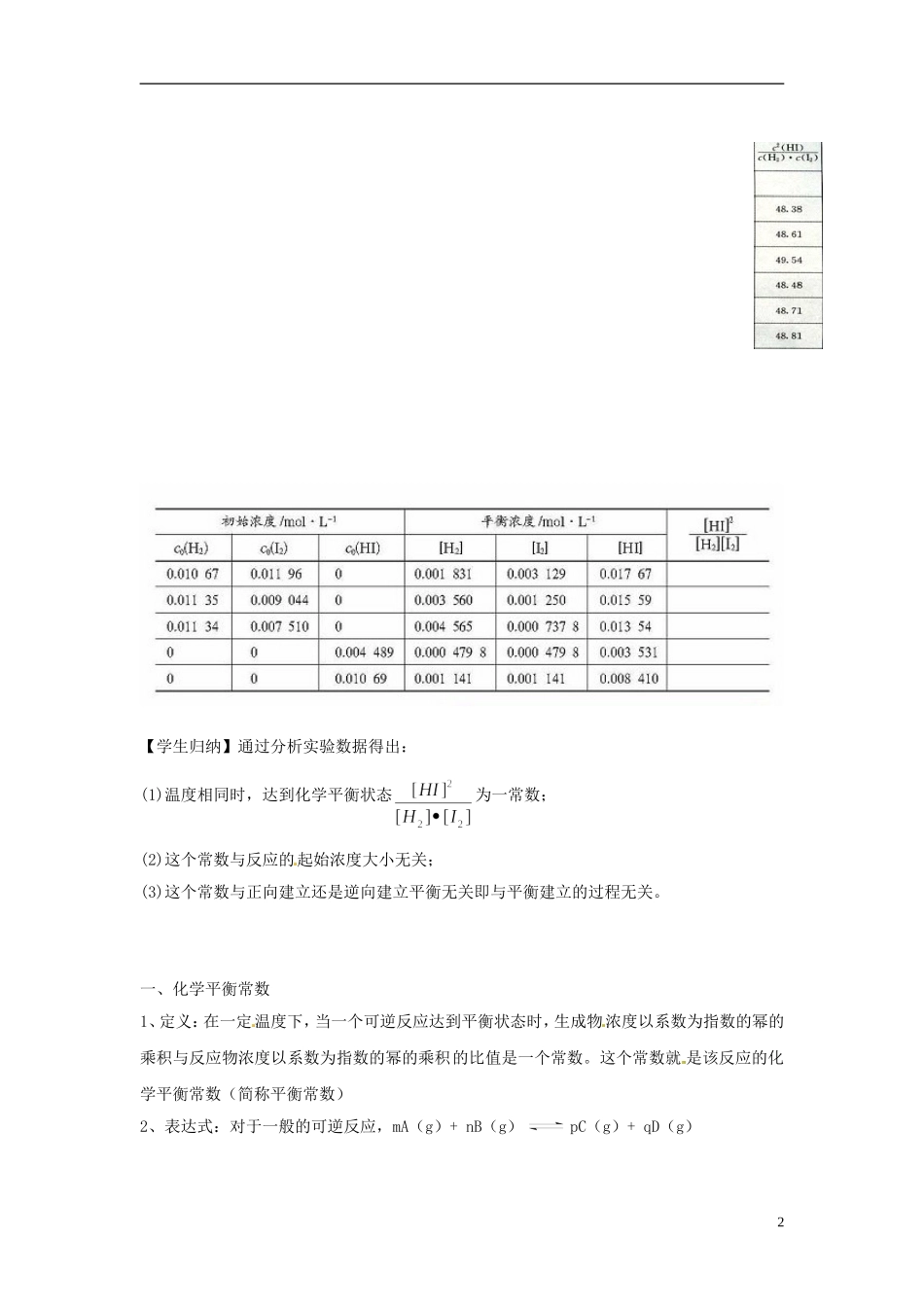
为更准确的了解可逆反应的进程,定量的描述化学反应的限度,我们将学习一个新的概念——化学平衡常数[学习新知识]当一个可逆反应达到化学平衡状态时,反应物和生成物的浓度之间有怎样的定量关系,请完成43页[交流与研讨],你能得出什么结论
1【学生归纳】通过分析实验数据得出:(1)温度相同时,达到化学平衡状态为一常数;(2)这个常数与反应的起始浓度大小无关;(3)这个常数与正向建立还是逆向建立平衡无关即与平衡建立的过程无关
一、化学平衡常数1、定义:在一定温度下,当一个可逆反应达到平衡状态时,生成物浓度以系数为指数的幂的乘积与反应物浓度以系数为指数的幂的乘积的比值是一个常数
这个常数就是该反应的化学平衡常数(简称平衡常数)2、表达式:对于一般的可逆反应,mA(g)+nB(g)pC(g)+qD(g)2当在一定温度下达到平衡时,K==引导学生完成44页【交流与研讨】1、2两题,你能得出什么结论
3、平衡常数的意义:(1)平衡常数的大小反映了化学反应进行的程度(也叫反应的限度)
K值越大,表示反应进