共价键第一课时教学目标:1、复习化学键的概念,能用电子式表示常见物质的离子键或共价键的形成过程
2、知道共价键的主要类型δ键和π键
3、说出δ键和π键的明显差别和一般规律
教学重点、难点:价层电子对互斥模型教学过程:[复习引入]NaCl、HCl的形成过程[设问]前面学习了电子云和轨道理论,对于HCl中H、Cl原子形成共价键时,电子云如何重叠
例:H2的形成[讲解、小结][板书]1、δ键:(以“头碰头”重叠形式)a、特征:以形成化学键的两原子核的连线为轴作旋转操作,共价键的图形不变,轴对称图形
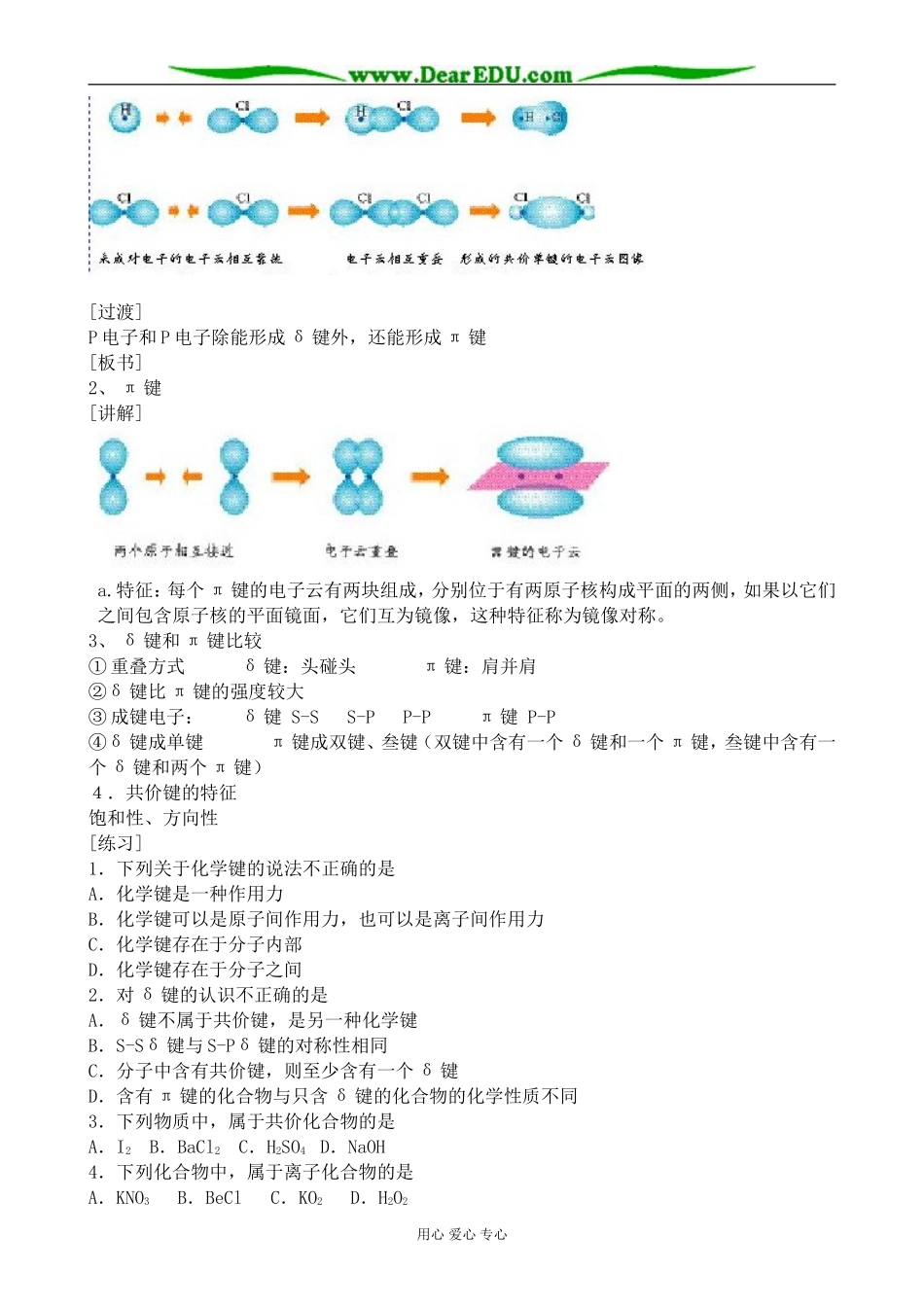
b、种类:S-Sδ键S-Pδ键P-Pδ键用心爱心专心[过渡]P电子和P电子除能形成δ键外,还能形成π键[板书]2、π键[讲解]a
特征:每个π键的电子云有两块组成,分别位于有两原子核构成平面的两侧,如果以它们之间包含原子核的平面镜面,它们互为镜像,这种特征称为镜像对称
3、δ键和π键比较①重叠方式δ键:头碰头π键:肩并肩②δ键比π键的强度较大③成键电子:δ键S-SS-PP-Pπ键P-P④δ键成单键π键成双键、叁键(双键中含有一个δ键和一个π键,叁键中含有一个δ键和两个π键)4.共价键的特征饱和性、方向性[练习]1.下列关于化学键的说法不正确的是A.化学键是一种作用力B.化学键可以是原子间作用力,也可以是离子间作用力C.化学键存在于分子内部D.化学键存在于分子之间2.对δ键的认识不正确的是A.δ键不属于共价键,是另一种化学键B.S-Sδ键与S-Pδ键的对称性相同C.分子中含有共价键,则至少含有一个δ键D.含有π键的化合物与只含δ键的化合物的化学性质不同3.下列物质中,属于共价化合物的是A.I2B.BaCl2C.H2SO4D.NaOH4.下列化合物中,属于离子化合物的是A.KNO3B.BeClC.KO2D.H2O2用心爱心专心5.写出下列物质的电子式
H2、N2、HCl、H2O6.用电子式