科目课题化学能与电能教学目标1、复习、巩固原电池的化学原理
2、正负极的判断电极反应式的书写,并学会应用
教材分析正负极的判断、电极反应式的书写,并学会应用
时序实施教学过程设计引入:在上一节课的学习中,我们了解了原电池反应原理和构成条件,这节课我们将继续学习原电池原理的应用
板书:第二章化学反应与能量第二节化学能与电能(第二课时)原电池的构成条件:这是一种把化学能转化为电能的装置
从理论上说,任何一个自发的氧化还原反应均可设计成原电池
负极与正极:作负极的一般是较活泼的金属材料,作正极的材料用一般导体即可
电解质溶液:c
闭合回路)原电池的工作原理:(1)电极反应(以铜锌原电池为例):负极:较活泼的金属或失去电子的一方Zn-2e-=Zn2+(氧化反应)正极:2H++2e-=H2↑(还原反应)(2)电子流向:从负极(Zn)流向正极(Cu)(3)电流方向:从正极(Cu)流向负极(Zn)(4)能量转变:将化学能转变成电能(课堂练习)判断这个原电池反应中的正负极,并书写电极反应式
若银片改为锌片呢
总结其中原电池两极的判断方法:活泼金属→发生氧化反应→向外线路提供电子→原电池的负极;不活泼金属(或石墨)→发生还原反应→接受外线路用心爱心专心提供的电子→原电池的正极
及根据总反应方程式书写原电池各电极反应式,提供反应方程式设计原电池、提供电极材料电解质溶液进行原电池是否形成的判断是重点
【科学探究】原电池的构成条件探究
[活动形式]学生分组实验
[实验类型]对比实验
[实验目的]使学生学会控制实验条件的方法
[探究活动组织]1
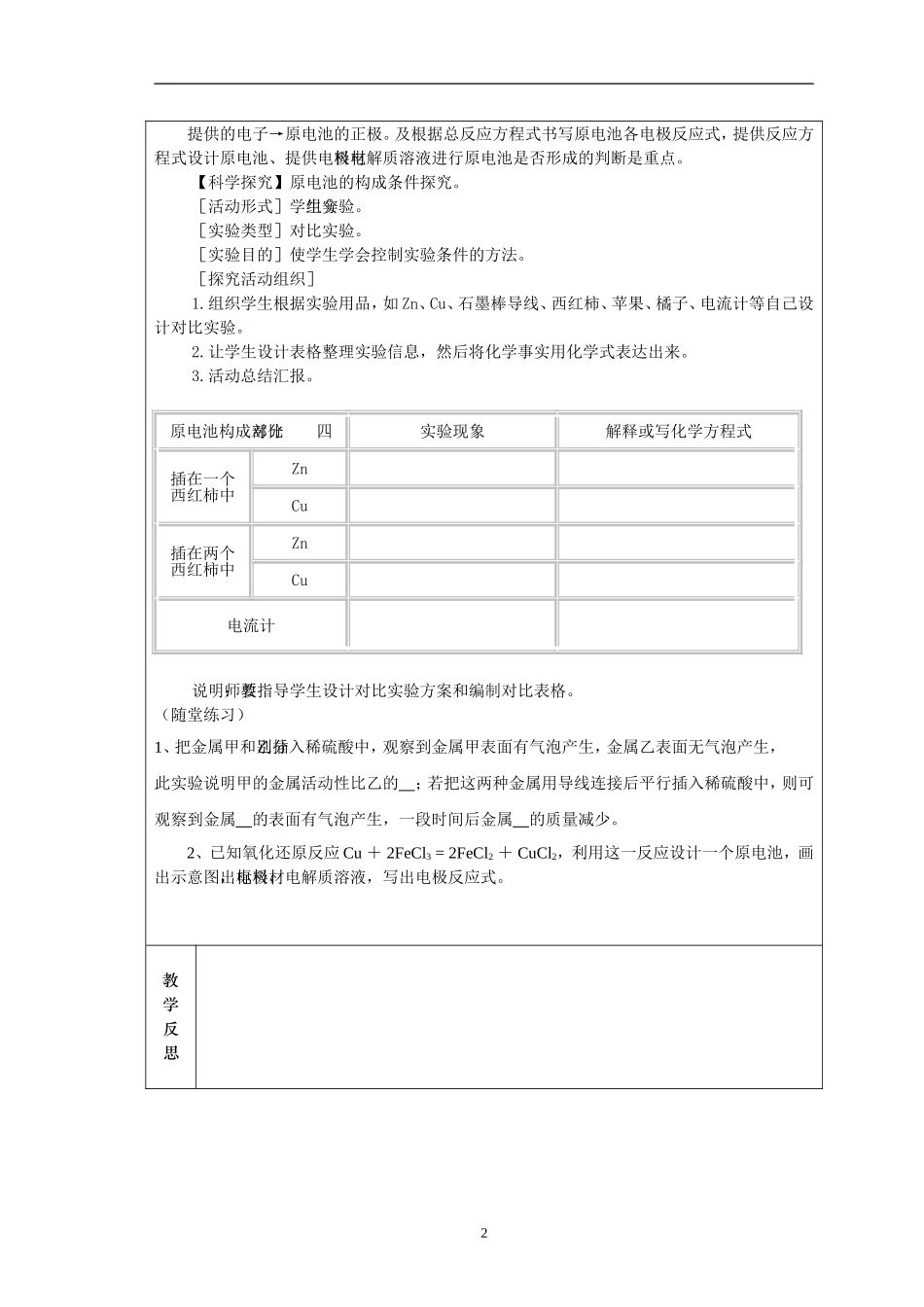
组织学生根据实验用品,如Zn、Cu、石墨棒导线、西红柿、苹果、橘子、电流计等自己设计对比实验
让学生设计表格整理实验信息,然后将化学事实用化学式表达出来
活动总结汇报
说明:教师要指导学生设计对比实验方案和编制对比表格
(随堂练习)1、把金属