专题2化学反应速率与化学平衡2
3化学平衡的移动(第2课时)压强变化对平衡浓度的影响教学课题专题专题2化学反应速率与化学平衡单元第三单元化学平衡的移动节题第二课时压强变化对平衡浓度的影响教学目标知识与技能通过实验探究压强对化学平衡的影响,并能用相关理论加以解释
过程与方法通过实验测定压强对化学平衡的影响,培养观察、记录实验现象及数据处理能力
情感态度与价值观通过压强对化学平衡的影响体会化学反应在生活、生活中的实际应用
教学重点探究压强对化学平衡的影响教学难点相关理论加以解释教学方法讨论法、探究法教学过程教师主导活动学生主体活动[回顾]1、什么叫平衡常数
写出其表达式
[交流与讨论]1、通过的方法增大压强,和同时增大
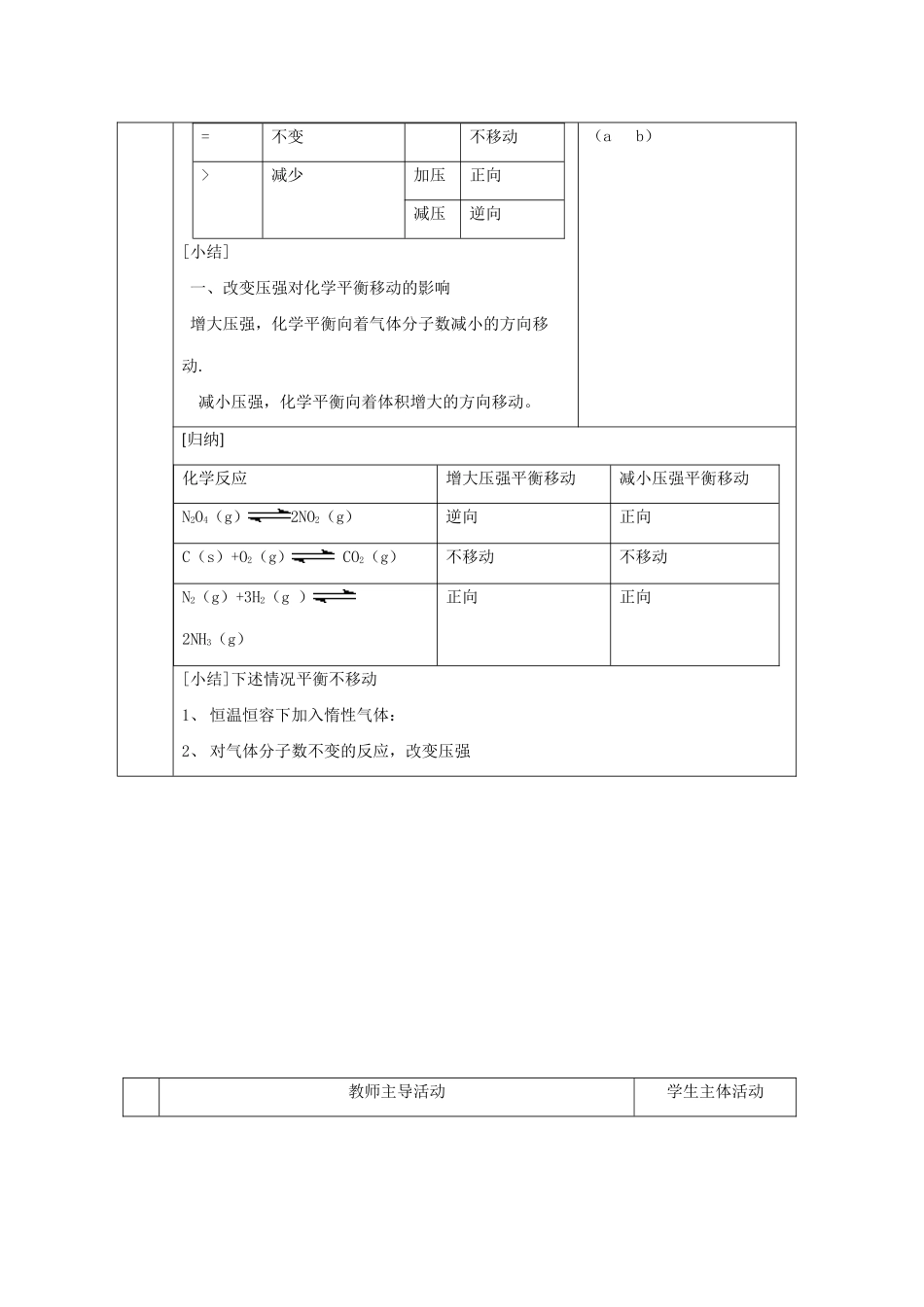
2、对于aA(g)bB(g)平衡常数表达式,a、b关系反应前后分子数改变压强变化平衡移动方向减少加压正向减压逆向[小结]一、改变压强对化学平衡移动的影响增大压强,化学平衡向着气体分子数减小的方向移动
减小压强,化学平衡向着体积增大的方向移动
(ab)[归纳]化学反应增大压强平衡移动减小压强平衡移动N2O4(g)2NO2(g)逆向正向C(s)+O2(g)CO2(g)不移动不移动N2(g)+3H2(g)2NH3(g)正向正向[小结]下述情况平衡不移动1、恒温恒容下加入惰性气体:2、对气体分子数不变的反应,改变压强教师主导活动学生主体活动教学过程[解释]观察、理解讨论后答出[典型例题]1、对于可逆反应2NO(g)+O2(g)2NO2(g),改变下列条件,平衡如何移动
(1)增大氧气浓度(2)增大压强(3)增大密闭容器的体积(4)向密闭容器中充入氮气[分析](1)正反应方向移动(2)正反应方向移动(气体分子数减少)(3)逆反应方向方向移动,增大体积相当于减小体积,向气体分子数增大的方向移动(4)平衡不移动
反应物、生成物的浓度不变(组分分压不变)板书计一、压强对化学平衡