第1课时利用化学反应制备物质[学习目标]1
掌握实验室制备氯气的原理、净化方法及尾气处理方法
了解常见气体的实验室制备装置及收集方法
了解一些常见物质的制备原理
一、氯气的制备方法[自主学习]1.氯气的实验室制法(1)试剂:□浓盐酸和□MnO2
(2)反应原理化学反应方程式:□MnO2+4HCl(浓)=====MnCl2+Cl2↑+2H2O
离子反应方程式:□MnO2+2Cl-+4H+=====Mn2++Cl2↑+2H2O
①氧化剂是□MnO2,还原剂是□HCl,氧化剂与还原剂的物质的量之比为□1∶2
②在MnO2与浓盐酸反应制取氯气的反应中体现了浓盐酸的□酸性、□氧化性
③若2molHCl参加反应,被氧化的HCl为□1mol
(3)反应特点固体+液体――→气体
(4)实验装置仪器名称:①□分液漏斗,②□圆底烧瓶
2.氯气的工业制法——电解饱和食盐水(1)化学方程式:□2NaCl+2H2O=====2NaOH+H2↑+Cl2↑
氧化剂是□H2O,还原剂是□NaCl
(2)离子方程式:□2Cl-+2H2O=====2OH-+H2↑+Cl2↑
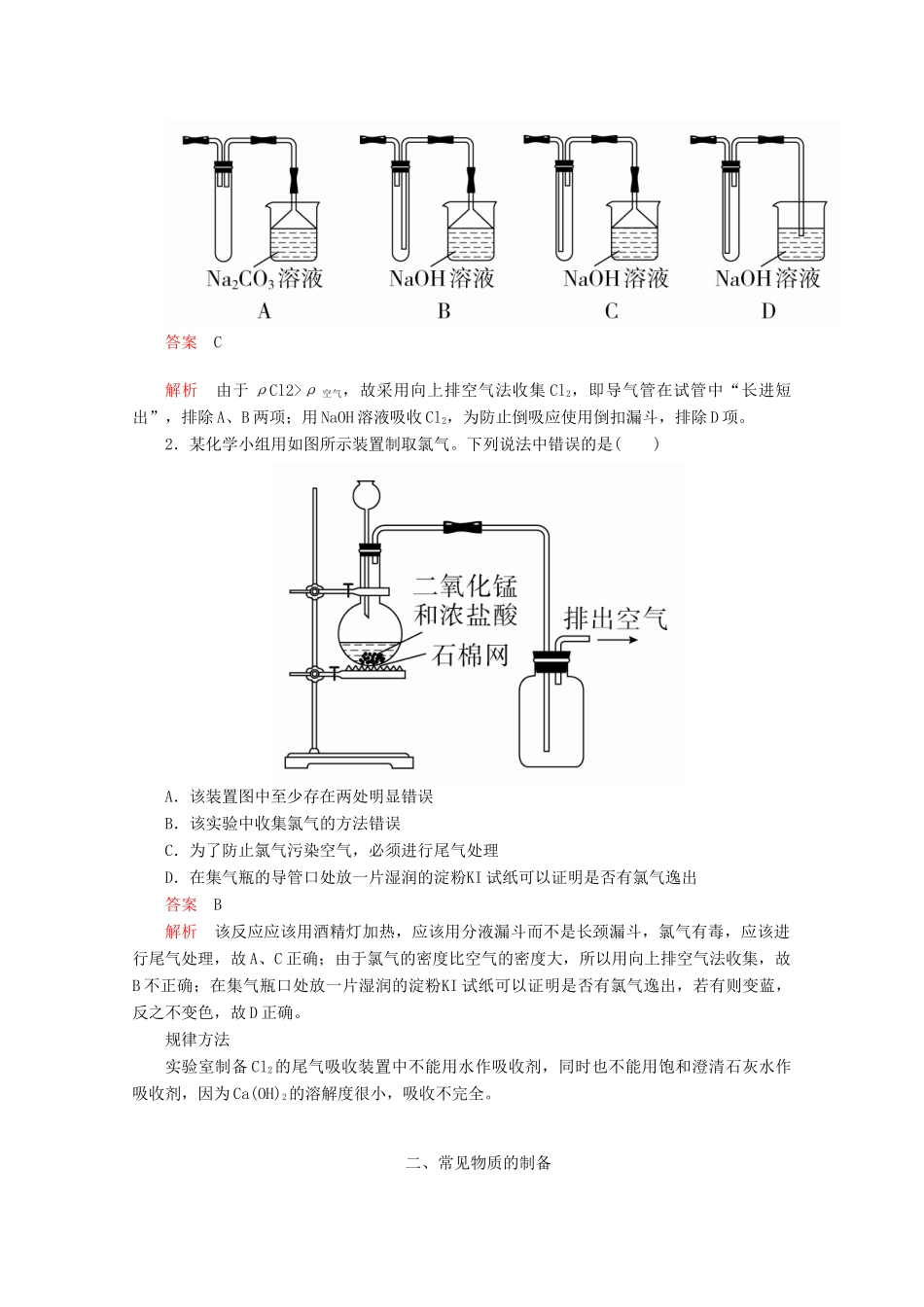
1.在实验室制备的Cl2中含有哪些杂质
为防止环境污染,多余的Cl2一般用什么试剂吸收
提示:HCl和水蒸气
分别通入装有饱和食盐水和浓硫酸的洗气瓶
多余的Cl2一般用NaOH溶液吸收,以防污染环境
2.从氧化还原反应知识的角度分析,工业上和实验室制备Cl2的反应原理有何异同
提示:两个反应原理的共同点是把-1价的Cl氧化成0价的Cl,不同点是工业上制备Cl2的氧化剂是H2O,还原剂是NaCl,实验室制备Cl2的氧化剂是MnO2,还原剂是HCl
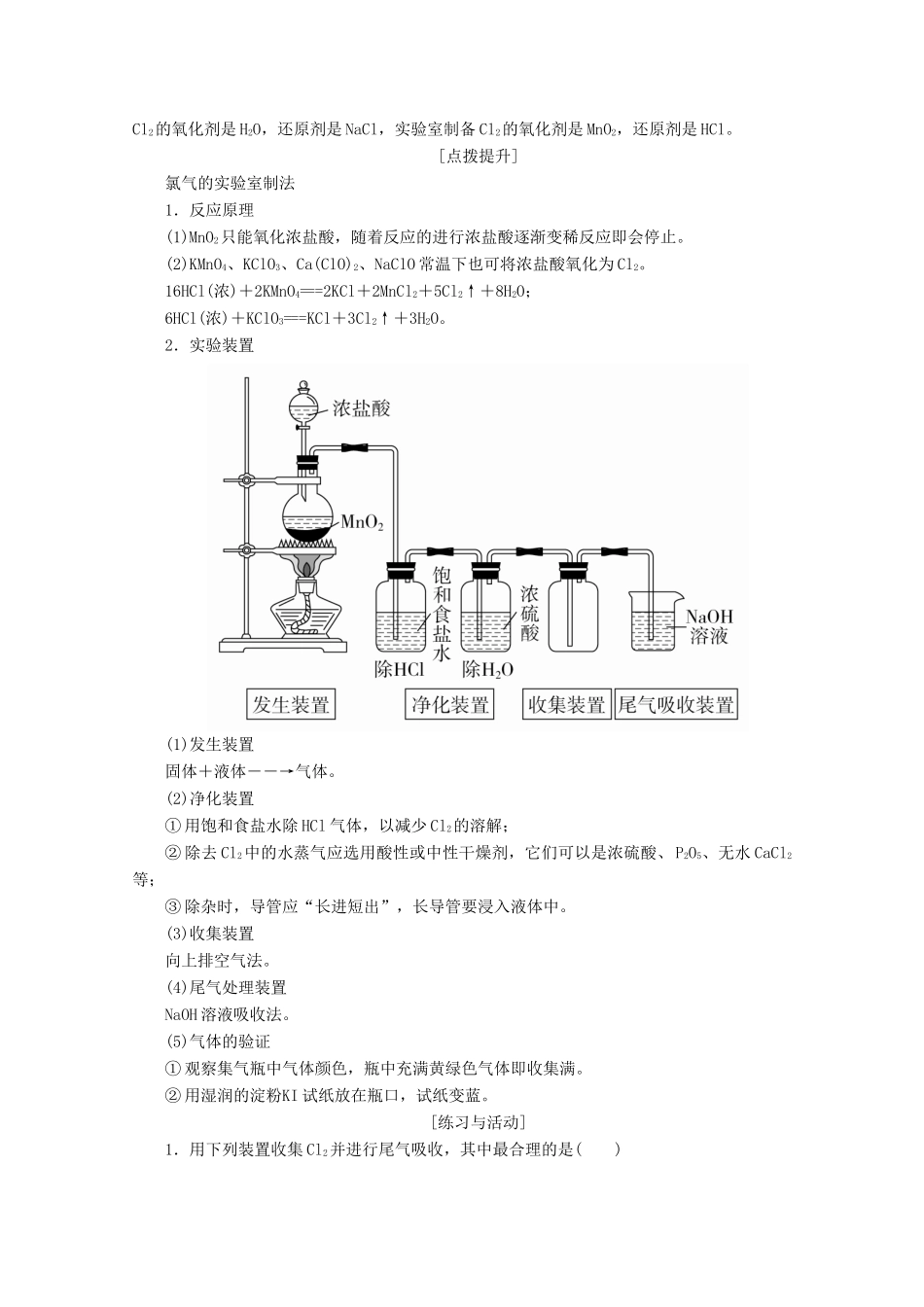
[点拨提升]氯气的实验室制法1.反应原理(1)MnO2只能氧化浓盐酸,随着反应的进行浓盐酸逐渐变稀反应即会停止
(2)KMnO4、KClO3、Ca(ClO)2、NaClO常温下