第二节化学计量在实验中的应用一、考纲要求1、理解原子量(相对原子质量),分子量(相对分子质量)的涵义
2、掌握物质的量、摩尔质量、物质的量浓度、气体摩尔体积的涵义
理解阿佛加德罗常数的涵义
掌握物质的量与微粒(原子、分子、离子等)数目,气体体积(标准状况下)之间的相互关系
3、掌握有关原子量、分子量,有关物质的量,有关气体摩尔体积,有关物质溶解度,有关溶液浓度(质量分数和物质的量浓度)的计算
一、摩尔:1、物质的量我们知道,物质都是由分子、原子、离子等微观粒子组成的
这些微粒非常小,质量很轻,难于称量
但是物质之间的反应,既是按照一定的微粒个数进行,又是以可称量的物质来进行反应的
这就需要一个物理量把微粒的多少与可称量的物质的质量联系起来,这个物理量就是“物质的量”,为了帮助同学尽快理解掌握这一概念,分析如下几点:(1)物质的量是国际单位制中七个基本物理量之一
七个基本物理量的名称、单位(SI单位)及单位符号物理量单位名称单位符号长度米m质量千克kg时间秒S电流安[培]A热力学温度开[尔文]K物质的量摩[尔]mol发光强度坎[德拉]cd(2)“物质的量”是表示物质所含微粒多少的物理量
如同长度、质量等物理量一样,“物质的量”这四个字不得简化,也不得增添任何字,不能多一个字,也不能少一个字,更不能把它当作表示物质数量或质量多少的量
它是表示微观粒子集体的一个物理量
2、摩尔(1)摩尔的概念摩尔是物质的量的单位
同其它物理量都有度量各自的单位一样,“物质的量”也有计量单位
正如米是长度的单位一样,摩尔是物质的量的单位
摩尔可简称为“摩”,其符号是“mol”
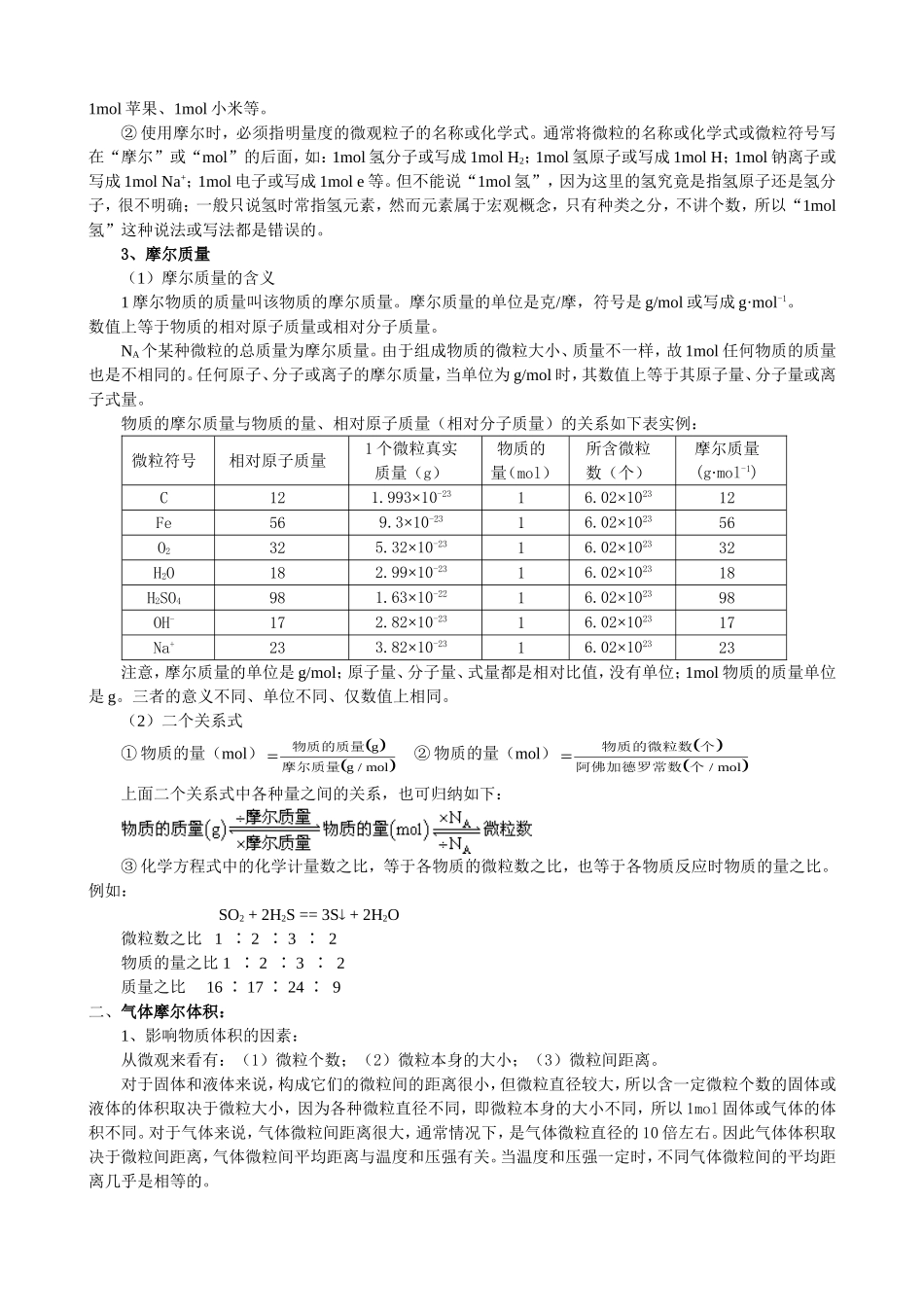
(2)摩尔的确定按规定,科学上应用0
012kg(即12g)碳12(指原子核内含6个质子和6个中子的一种碳原子,通常表示为12C或612C)所含碳原子数目就是1摩尔
也就是说,摩尔这个单位是以0
012kg12C所含的原子