第2课时共价晶体发展目标体系构建1
借助共价晶体模型认识共价晶体的结构特点
能够从化学键的特征,分析理解共价晶体的物理特性
一、共价晶体的结构和性质1.共价晶体的结构特点(1)构成粒子及作用力共价晶体(2)空间结构:整块晶体是一个三维的共价键网状结构,不存在单个的小分子,是一个“巨分子”
2.共价晶体与物质的类别物质种类实例某些非金属单质晶体硼、晶体硅、晶体锗、金刚石等某些非金属化合物碳化硅(SiC)、氮化硅(Si3N4)、氮化硼(BN)等某些氧化物二氧化硅(SiO2)等3
共价晶体的熔、沸点(1)共价晶体由于原子间以较强的共价键相结合,熔化时必需破坏共价键,而破坏它们需要很高的温度,所以共价晶体具有很高的熔点
(2)结构相似的共价晶体,原子半径越小,键长越短,键能越大,晶体的熔点越高
微点拨:含有共价键的晶体都是共价晶体吗
提示:共价晶体中都有共价键,但含有共价键的不一定是共价晶体
如CO2、H2O等分子晶体中也含有共价键
二、典型的共价晶体1.金刚石(1)碳原子采取sp3杂化,C—C—C夹角为109°28′
(2)每个碳原子与周围紧邻的4个碳原子以共价键结合成正四面体结构,向空间伸展形成空间网状结构
(3)最小碳环由6个碳原子组成,且最小环上有4个碳原子在同一平面内;每个碳原子被12个六元环共用
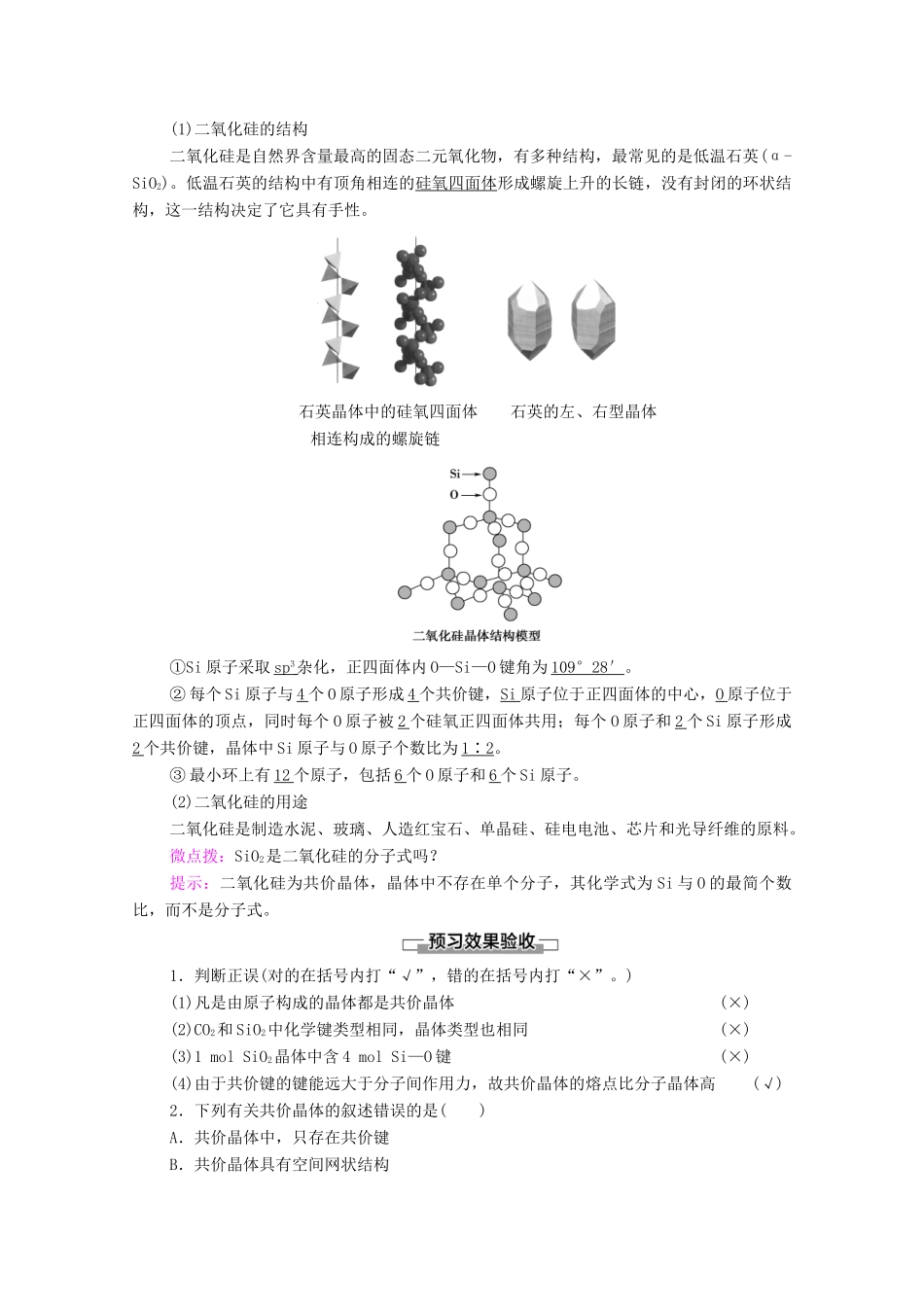
2.二氧化硅晶体(1)二氧化硅的结构二氧化硅是自然界含量最高的固态二元氧化物,有多种结构,最常见的是低温石英(α-SiO2)
低温石英的结构中有顶角相连的硅氧四面体形成螺旋上升的长链,没有封闭的环状结构,这一结构决定了它具有手性
石英晶体中的硅氧四面体石英的左、右型晶体相连构成的螺旋链①Si原子采取sp3杂化,正四面体内O—Si—O键角为109°28′
②每个Si原子与4个O原子形成4个共价键,Si原子位于正四面体的中心,O原子位于正四面体的顶点,同时每个O原子被2个硅氧正