专题二化学计量及其应用【考纲要求】1.了解物质的量、摩尔质量、气体摩尔体积、物质的量浓度、阿伏加德罗常数的含义
2.根据物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)等之间的相互关系进行有关计算
3.掌握利用化学方程式或离子方程式的计算
理解质量守恒定律的含义
4.了解物质的量浓度、溶液中溶质的质量分数的含义及其有关计算
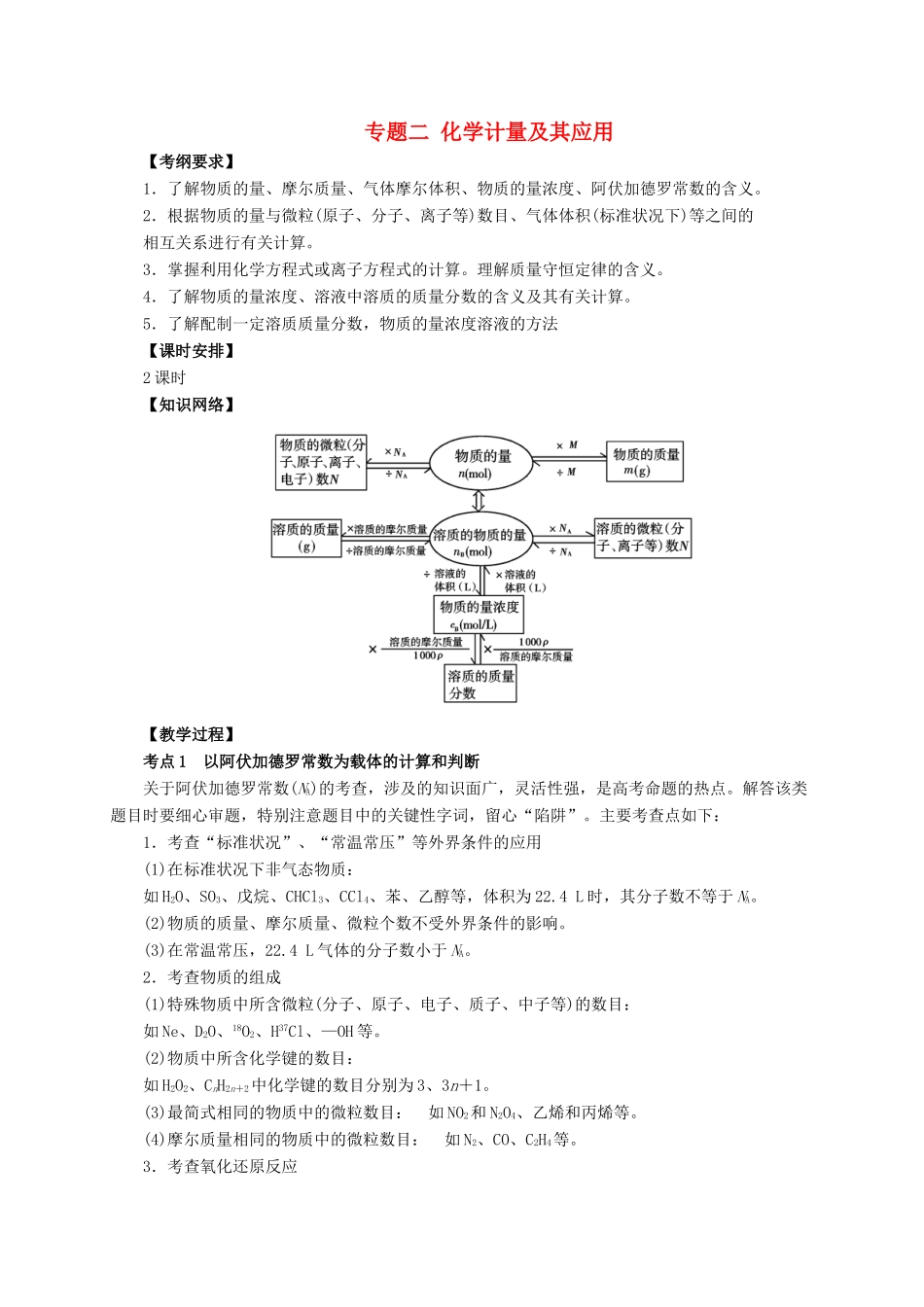
5.了解配制一定溶质质量分数,物质的量浓度溶液的方法【课时安排】2课时【知识网络】【教学过程】考点1以阿伏加德罗常数为载体的计算和判断关于阿伏加德罗常数(NA)的考查,涉及的知识面广,灵活性强,是高考命题的热点
解答该类题目时要细心审题,特别注意题目中的关键性字词,留心“陷阱”
主要考查点如下:1.考查“标准状况”、“常温常压”等外界条件的应用(1)在标准状况下非气态物质:如H2O、SO3、戊烷、CHCl3、CCl4、苯、乙醇等,体积为22
4L时,其分子数不等于NA
(2)物质的质量、摩尔质量、微粒个数不受外界条件的影响
(3)在常温常压,22
4L气体的分子数小于NA
2.考查物质的组成(1)特殊物质中所含微粒(分子、原子、电子、质子、中子等)的数目:如Ne、D2O、18O2、H37Cl、—OH等
(2)物质中所含化学键的数目:如H2O2、CnH2n+2中化学键的数目分别为3、3n+1
(3)最简式相同的物质中的微粒数目:如NO2和N2O4、乙烯和丙烯等
(4)摩尔质量相同的物质中的微粒数目:如N2、CO、C2H4等
3.考查氧化还原反应电子转移(得失)数目问题的分析,如Na2O2、NO2与H2O反应;电解AgNO3溶液、CuSO4溶液的反应;Cl2与NaOH、Fe反应等,分析该类题目时还要注意反应产物以及过量计算问题
4.考查弱电解质的电离、盐类的水解弱电解质在水溶液中部分电离,可水解的盐溶液中,离子发生微弱水解