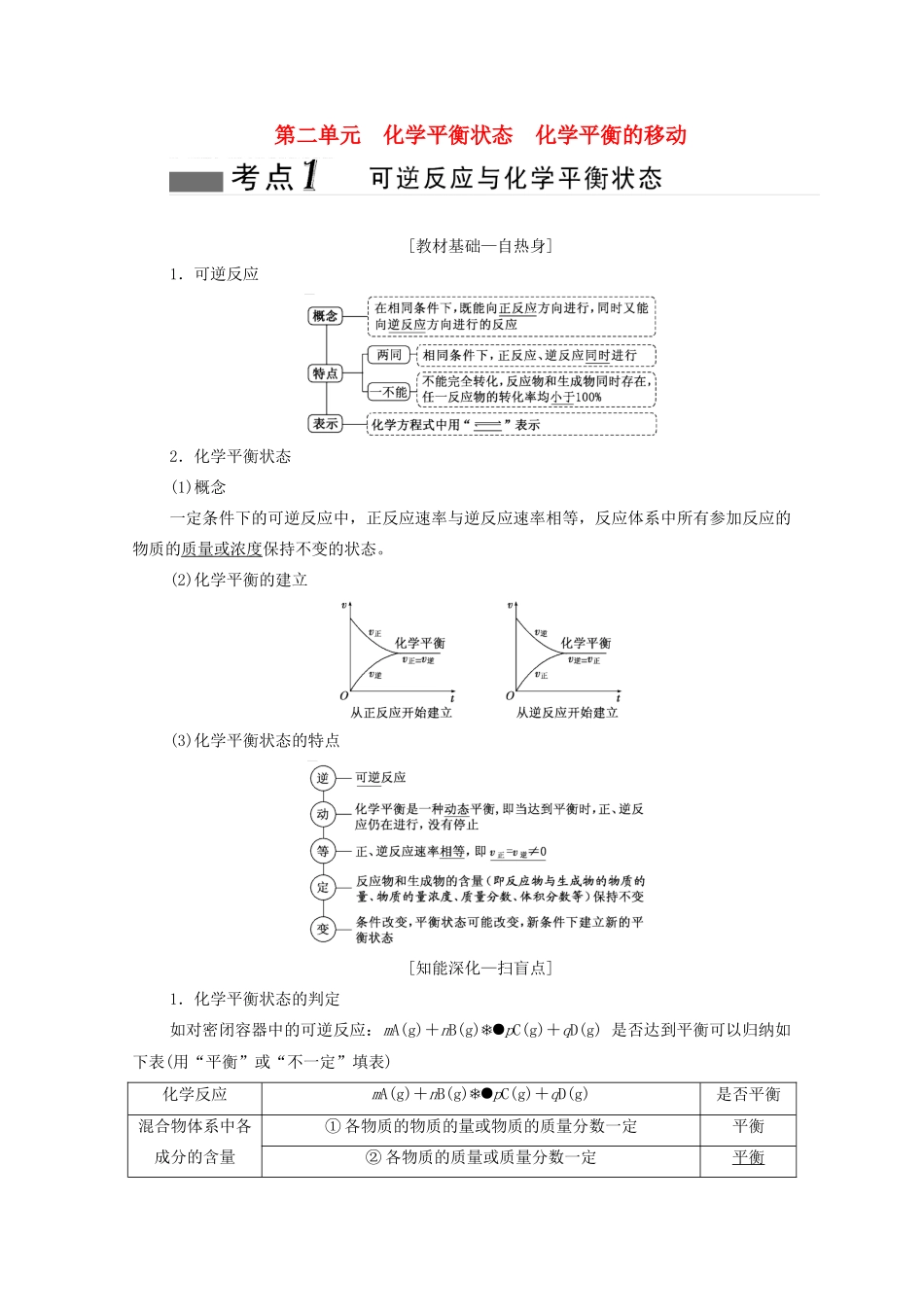
第二单元化学平衡状态化学平衡的移动[教材基础—自热身]1.可逆反应2.化学平衡状态(1)概念一定条件下的可逆反应中,正反应速率与逆反应速率相等,反应体系中所有参加反应的物质的质量或浓度保持不变的状态
(2)化学平衡的建立(3)化学平衡状态的特点[知能深化—扫盲点]1.化学平衡状态的判定如对密闭容器中的可逆反应:mA(g)+nB(g)pC(g)+qD(g)是否达到平衡可以归纳如下表(用“平衡”或“不一定”填表)化学反应mA(g)+nB(g)pC(g)+qD(g)是否平衡混合物体系中各成分的含量①各物质的物质的量或物质的质量分数一定平衡②各物质的质量或质量分数一定平衡③各气体的体积或体积分数一定平衡④总体积、总压强、总物质的量一定不一定正、逆反应速率之间的关系①在单位时间内消耗了mmolA,同时也生成了mmolA平衡②在单位时间内消耗了nmolB,同时也消耗了pmolC平衡③v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q不一定④在单位时间内生成了nmolB,同时也消耗了qmolD不一定压强①其他条件一定、总压强一定,且m+n≠p+q平衡②其他条件一定、总压强一定,且m+n=p+q不一定混合气体的平均相对分子质量①平均相对分子质量一定,且m+n≠p+q平衡②平均相对分子质量一定,且m+n=p+q不一定温度任何化学反应都随着能量变化,当体系温度一定时平衡气体的密度密度一定不一定颜色对于有色物质参加或生成的可逆反应,反应体系内有色物质的颜色稳定不变平衡化学键对同一物质而言,断裂的化学键的物质的量与形成的化学键的物质的量相等
如反应N2(g)+3H2(g)2NH3(g),若有下列各项成立a.断裂1molN≡N键的同时生成1molN≡N键;b.断裂1molN≡N键的同时生成3molH—H键;c.生成1molN≡N键的同时生成6molN—H键平衡2
以下几种情况不能作为