化学工艺流程[全国卷]1.(2018·全国卷Ⅱ)我国是世界上最早制得和使用金属锌的国家
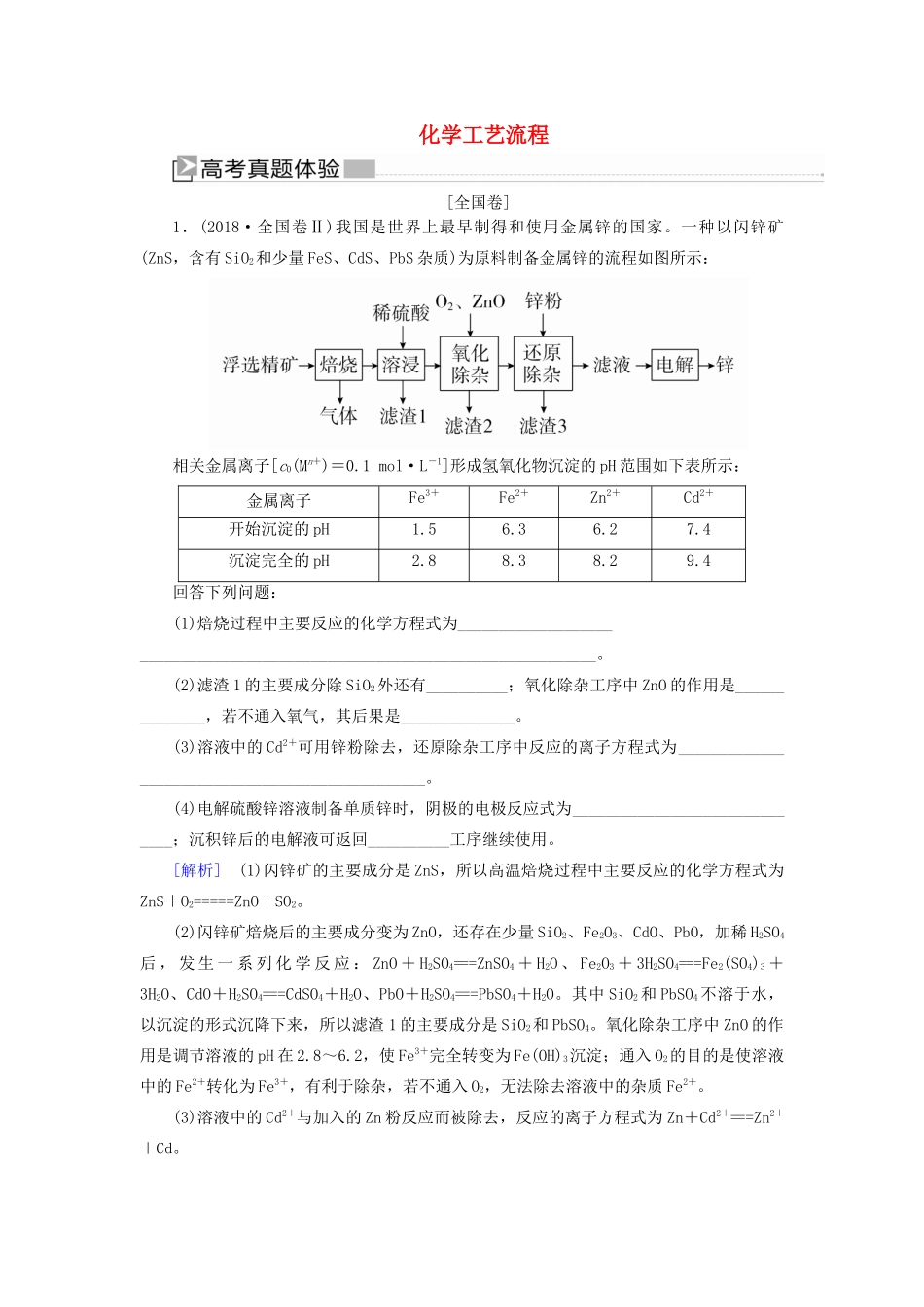
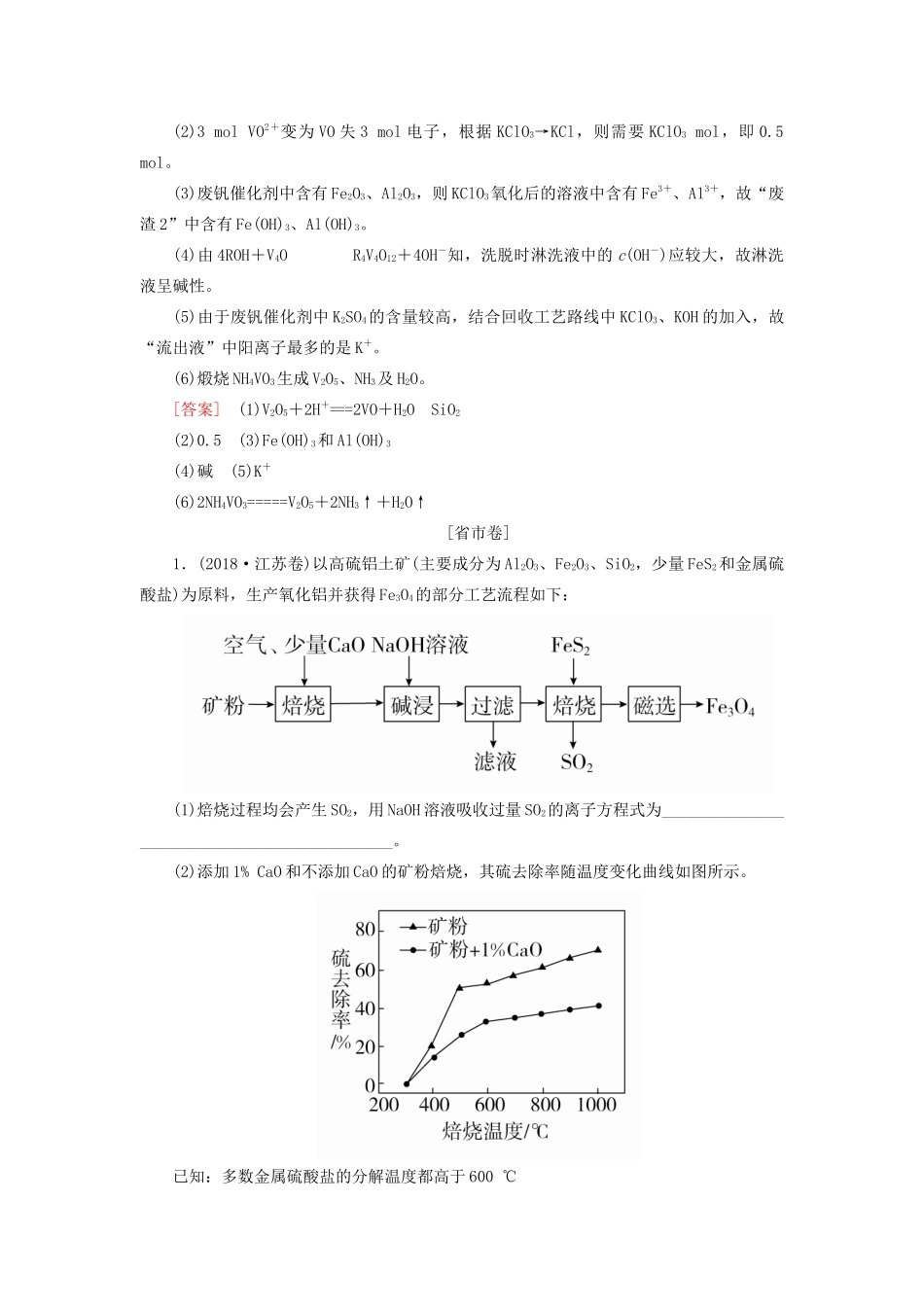
一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:相关金属离子[c0(Mn+)=0
1mol·L-1]形成氢氧化物沉淀的pH范围如下表所示:金属离子Fe3+Fe2+Zn2+Cd2+开始沉淀的pH1
4沉淀完全的pH2
4回答下列问题:(1)焙烧过程中主要反应的化学方程式为___________________________________________________________________________
(2)滤渣1的主要成分除SiO2外还有__________;氧化除杂工序中ZnO的作用是______________,若不通入氧气,其后果是______________
(3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为________________________________________________
(4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为______________________________;沉积锌后的电解液可返回__________工序继续使用
[解析](1)闪锌矿的主要成分是ZnS,所以高温焙烧过程中主要反应的化学方程式为ZnS+O2=====ZnO+SO2
(2)闪锌矿焙烧后的主要成分变为ZnO,还存在少量SiO2、Fe2O3、CdO、PbO,加稀H2SO4后,发生一系列化学反应:ZnO+H2SO4===ZnSO4+H2O、Fe2O3+3H2SO4===Fe2(SO4)3+3H2O、CdO+H2SO4===CdSO4+H2O、PbO+H2SO4===PbSO4+H2O
其中SiO2和PbSO4不溶于水,以沉淀的形式沉降下来,所以