专题五物质结构元素周期律【考纲要求】1
了解元素、核素和同位素的含义
了解原子构成、原子核外电子排布
掌握元素周期律的实质
以第3周期、ⅠA和ⅦA族为例,掌握同一周期同一主族内元素性质递变规律与原子结构的关系
了解化学键的定义
知道离子键、共价键的形成和存在的物质类别
了解原子结构示意图、分子式、电子式、结构式及其简式的表示方法
【课时安排】2课时【考情分析】历年高考本部分知识都有考查,主要有三个方面:一、结构和组成,包括原子、分子和物质结构,重点是原子结构,通常从核素、核外电子排布与数目等角度考查;二、元素周期律和元素周期表,包括元素在周期表中位置的判断、元素性质的比较以及周期律的应用等;三、微粒间的作用力,主要涉及到离子键和共价键的比较和判断
【教学过程】考点1:原子结构核外电子排布一、知识梳理1
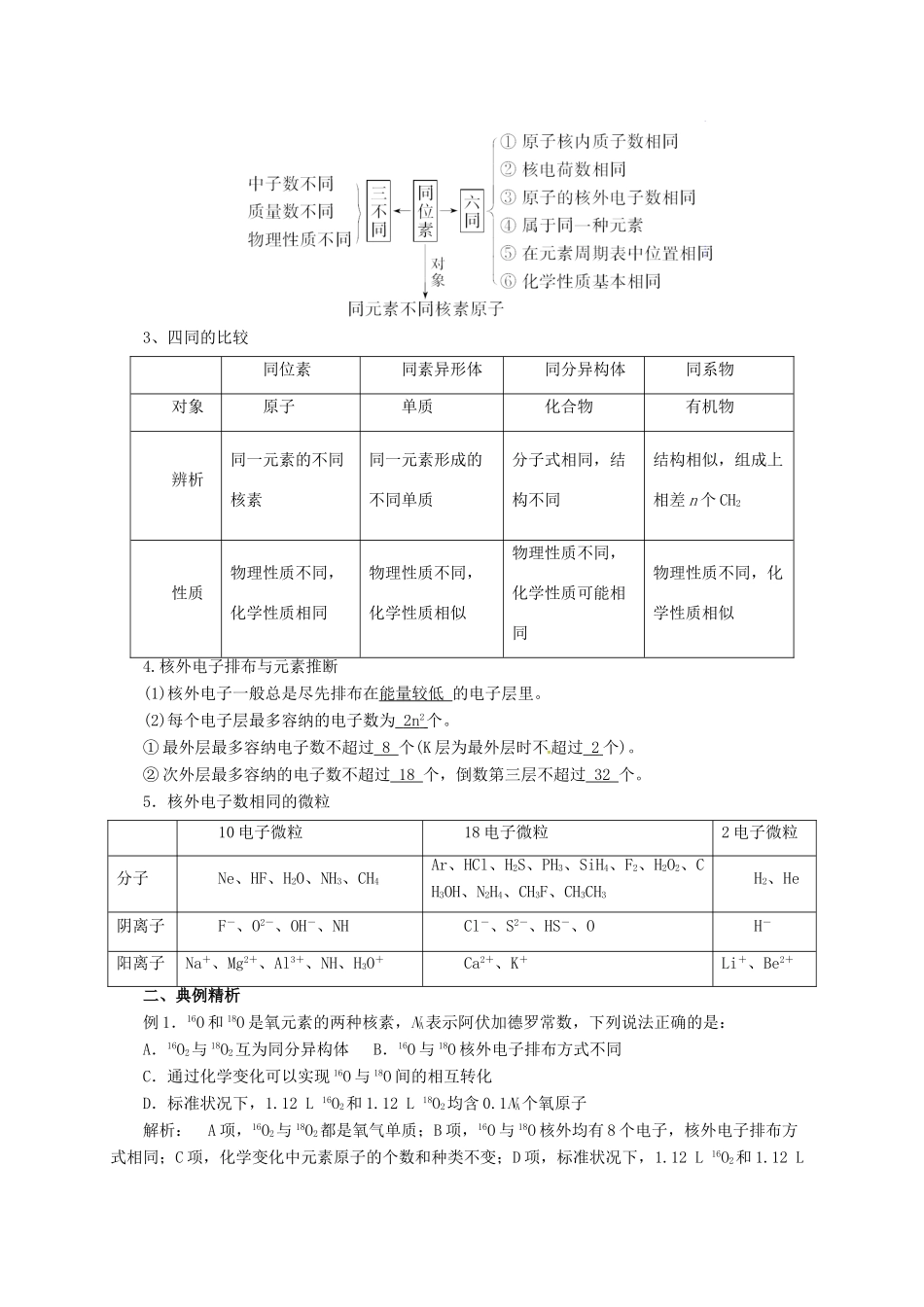
原子的组成和结构(1)(2)有关粒子间的关系①质子数(Z)=核电荷数=原子的核外电子数=原子序数②质量数(A)=质子数(Z)+中子数(N)③阳离子的核外电子数=质子数-电荷数④阴离子的核外电子数=质子数+电荷数2.同位素的六同和三不同3、四同的比较同位素同素异形体同分异构体同系物对象原子单质化合物有机物辨析同一元素的不同核素同一元素形成的不同单质分子式相同,结构不同结构相似,组成上相差n个CH2性质物理性质不同,化学性质相同物理性质不同,化学性质相似物理性质不同,化学性质可能相同物理性质不同,化学性质相似4
核外电子排布与元素推断(1)核外电子一般总是尽先排布在能量较低的电子层里
(2)每个电子层最多容纳的电子数为2n2个
①最外层最多容纳电子数不超过8个(K层为最外层时不超过2个)
②次外层最多容纳的电子数不超过18个,倒数第三层不超过32个
5.核外电子数相同的微粒10电子微粒18电子微粒2电子微粒分子Ne、HF、H2O、NH3、CH4Ar、HCl、H2S