化学反应原理综合[全国卷]1.(2019·全国卷Ⅰ)水煤气变换[CO(g)+H2O(g)===CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中
回答下列问题:(1)Shibata曾做过下列实验:①使纯H2缓慢地通过处于721℃下的过量氧化钻CoO(s),氧化钴部分被还原为金属钴Co(s),平衡后气体中H2的物质的量分数为0
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0
根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO________H2(填“大于”或“小于”)
(2)721℃时,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,采用适当的催化剂进行反应,则平衡时体系中H2的物质的量分数为________(填标号)
50(3)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注
可知水煤气变换的ΔH________0(填“大于”“等于”或“小于”)
该历程中最大能垒(活化能)E正________eV,写出该步骤的化学方程式_____________________________________________
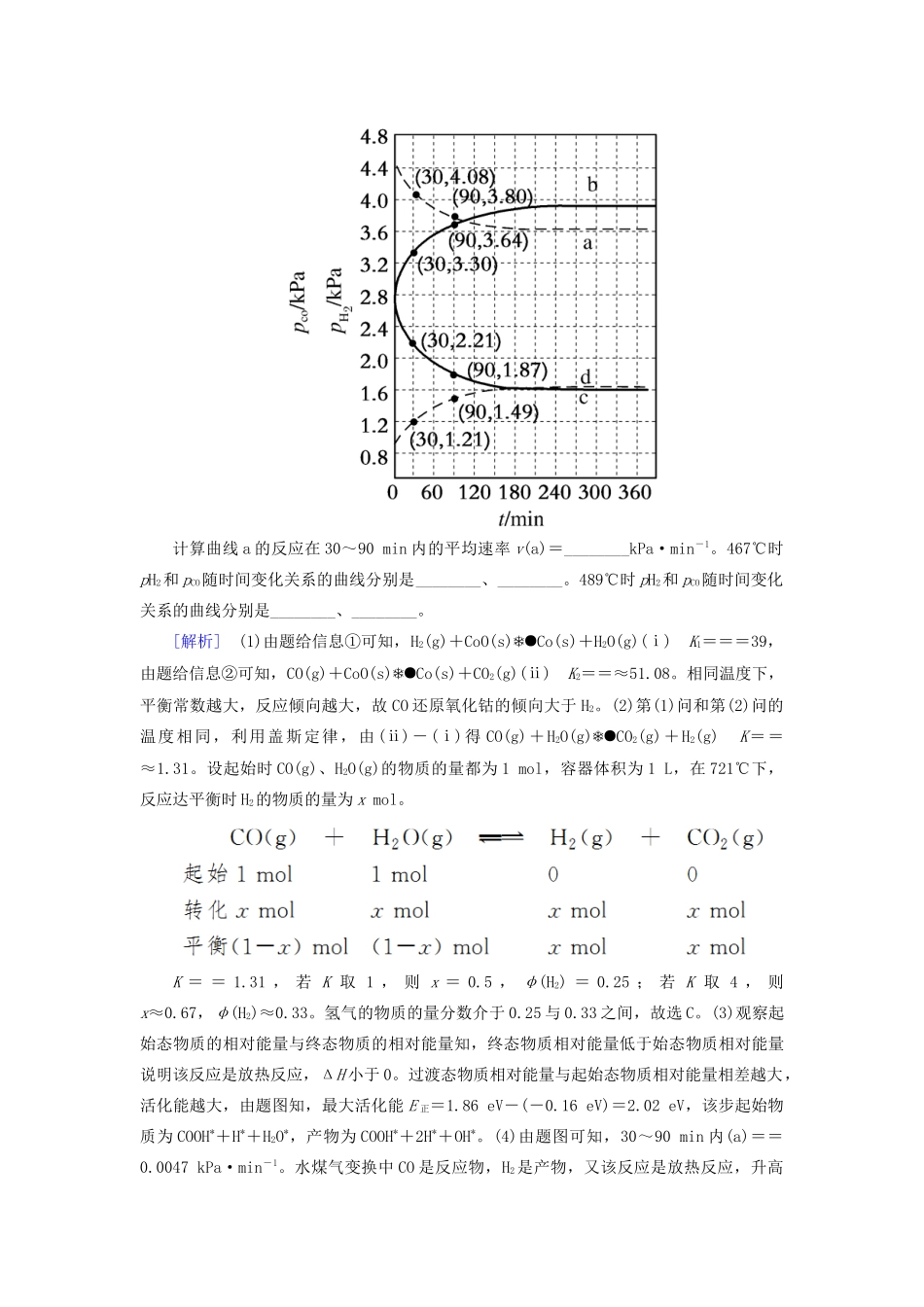
(4)Shoichi研究了467℃、489℃时水煤气变换中CO和H2分压随时间变化关系(如图所示),催化剂为氧化铁,实验初始时体系中的pH2O和pCO相等、pCO2和pH2相等
计算曲线a的反应在30~90min内的平均速率v(a)=________kPa·min-1
467℃时pH2和pCO随时间变化关系的曲线分别是________、________
489℃时pH2和pCO随时间变化关系的曲线分别是________、________
[解析](1)由题给信息①可知,H2(g)