第4节化学反应条件的优化——工业合成氨1.(重知道如何应用化学反应速率和化学平衡原理,选择合成氨的适宜条件
点)2.初步学会应用化学原理选择化工生产条件的思想和方法
(难点)工业合成氨[基础·初探]教材整理1合成氨反应的限度1.反应原理N2(g)+3H2(g)198
2J·mol-1·K-1
2.反应特点合成氨反应是一个能自发进行的、放热的、气体体积减小的可逆反应
3.有利于氨生成的措施(1)降低温度、增大压强有利于化学平衡向生成氨的方向移动
(2)在一定的温度和压强下,反应物中N2和H2的体积比为1∶3时平衡混合物中氨的含量最高
教材整理2合成氨反应的速率1.浓度在特定条件下,合成氨反应的速率与参加反应的物质的浓度的关系式为v=kc(N2)·c1
5(H2)·c-1(NH3),由关系式可知,增大N2或H2的浓度,减小NH3的浓度,都有利于提高合成氨的速率
2.催化剂使用催化剂,可显著降低反应的活化能,使反应速率提高上万亿倍
3.温度温度对合成氨反应的速率也有显著影响:温度越高,反应进行得越快
4.压强压强越大,反应进行得越快
12NH3(g)298K时ΔH=-92
2kJ·mol-1ΔS=-教材整理3合成氨的适宜条件1.合成氨反应条件的选择工业生产中,必须从反应速率和反应限度两个角度选择合成氨的适宜条件,既要考虑尽量增大反应物的转化率,充分利用原料,又要选择较快的反应速率,提高单位时间内的产量,同时还要考虑设备的要求和技术条件
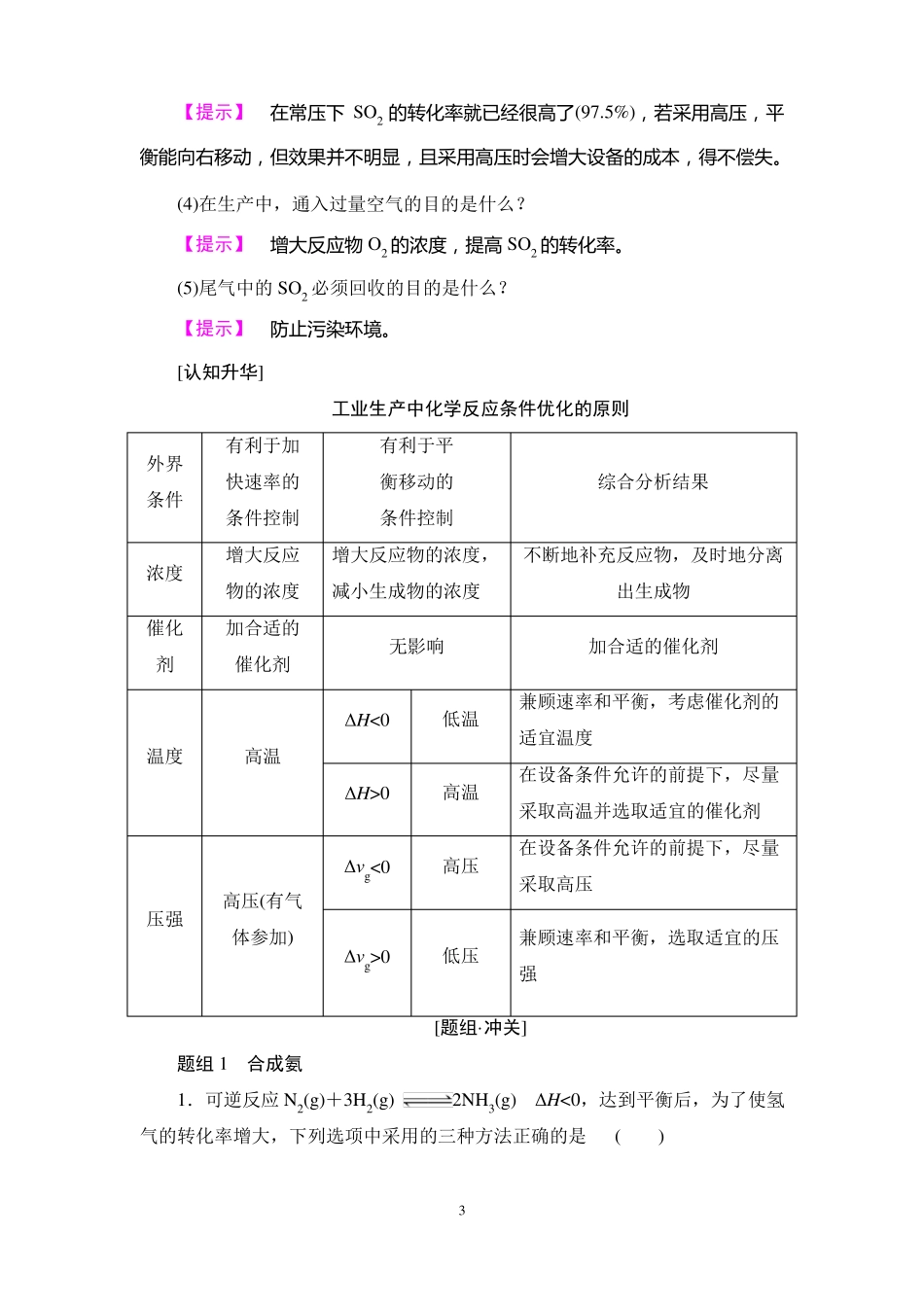
2.合成氨的适宜条件压强反应条件1×10~1×10Pa87温度催化剂浓度使气态NH3变成液态NH3700K左右铁触媒(铁)并及时从平衡混合物中分离出去,及时补充N2和H2[探究·升华][思考探究]在硫酸工业中,通过下列反应使SO2氧化成SO3:2SO2(g)+O2(g)2SO3(g)ΔH=-198kJ·mol-1
(已知催化剂是V2O5,在400~