第二节氧化还原反应【能力目标】1.了解化学反应基本类型,掌握氧化还原反应的基本分析方法
2.掌握氧化还原反应实质,氧化剂和还原剂的判断
3.掌握用化合价升降法配平氧化还原反应方程式
4.掌握氧化还原反应基本计算的规律
5.通过复习培养学生的判断能力和应用能力
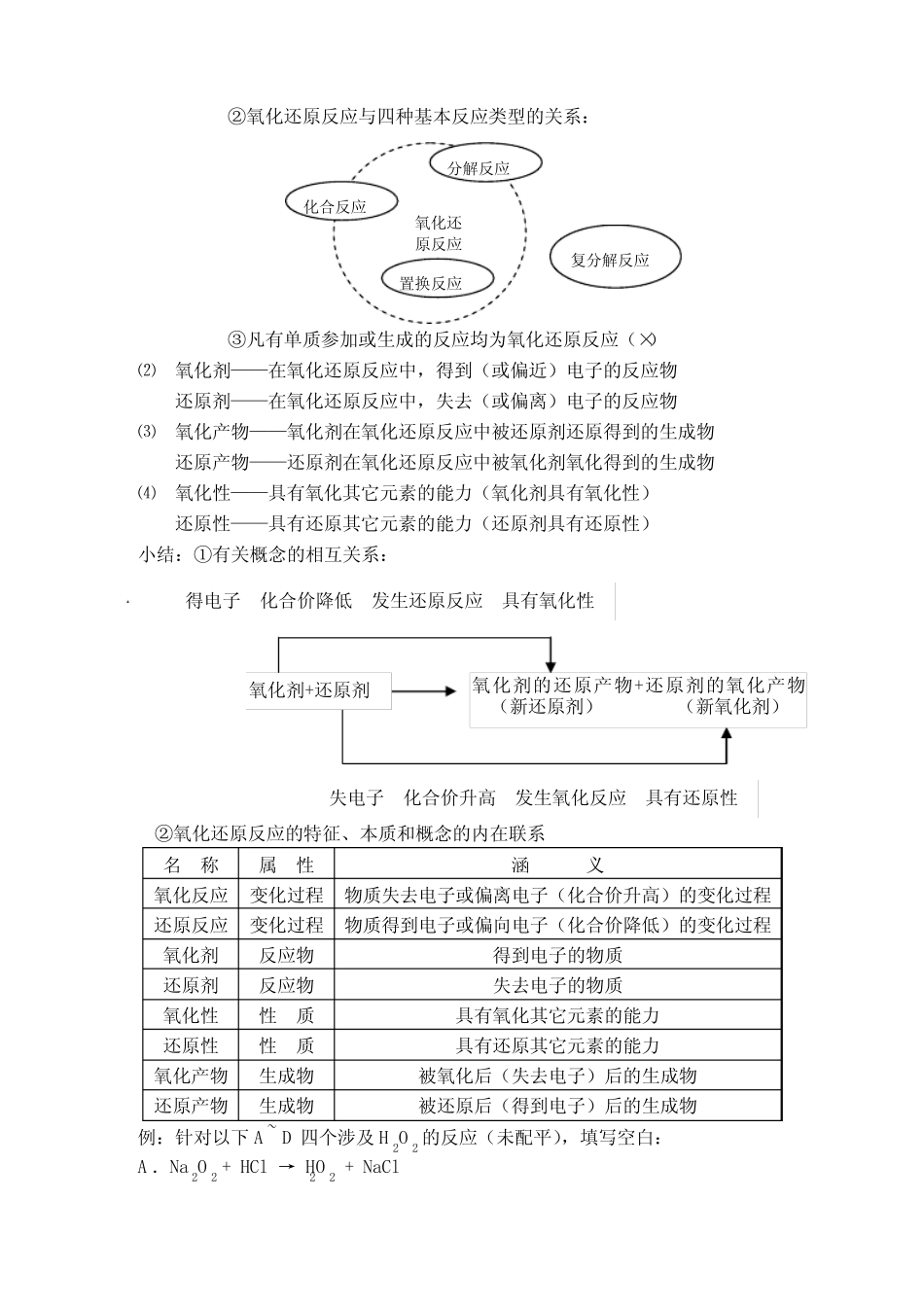
【能力培养】化学反应的分类1、概念⑴氧化反应——物质失去(或偏离)电子的反应还原反应——物质得到(或偏近)电子的反应氧化还原反应——凡有电子转移(得失或偏移)的化学反应实质:有电子转移(得失与偏移)特征:反应前后元素化合价有变化(亦为氧化还原反应的判断依据)讨论:①H2与Cl2发生化学反应时,氢元素失去电子,化合价升高被氧化(×)四种基本类型化合反应分解反应置换反应复分解反应电子转移氧化还原反应非氧化还原反应是否有离子参加反应离子反应分子反应反应进行程度可逆反应不可逆反应反应的热效应放热反应吸热反应②氧化还原反应与四种基本反应类型的关系:③凡有单质参加或生成的反应均为氧化还原反应(×)⑵氧化剂——在氧化还原反应中,得到(或偏近)电子的反应物还原剂——在氧化还原反应中,失去(或偏离)电子的反应物⑶氧化产物——氧化剂在氧化还原反应中被还原剂还原得到的生成物还原产物——还原剂在氧化还原反应中被氧化剂氧化得到的生成物⑷氧化性——具有氧化其它元素的能力(氧化剂具有氧化性)还原性——具有还原其它元素的能力(还原剂具有还原性)小结:①有关概念的相互关系:②氧化还原反应的特征、本质和概念的内在联系名称属性涵义氧化反应变化过程物质失去电子或偏离电子(化合价升高)的变化过程还原反应变化过程物质得到电子或偏向电子(化合价降低)的变化过程氧化剂反应物得到电子的物质还原剂反应物失去电子的物质氧化性性质具有氧化其它元素的能力还原性性质具有还原其它元素的能力氧化产物生成物被氧化后(失去电子)后的生成物还原产物生成物被还原后(得到电子)后的生成物例: