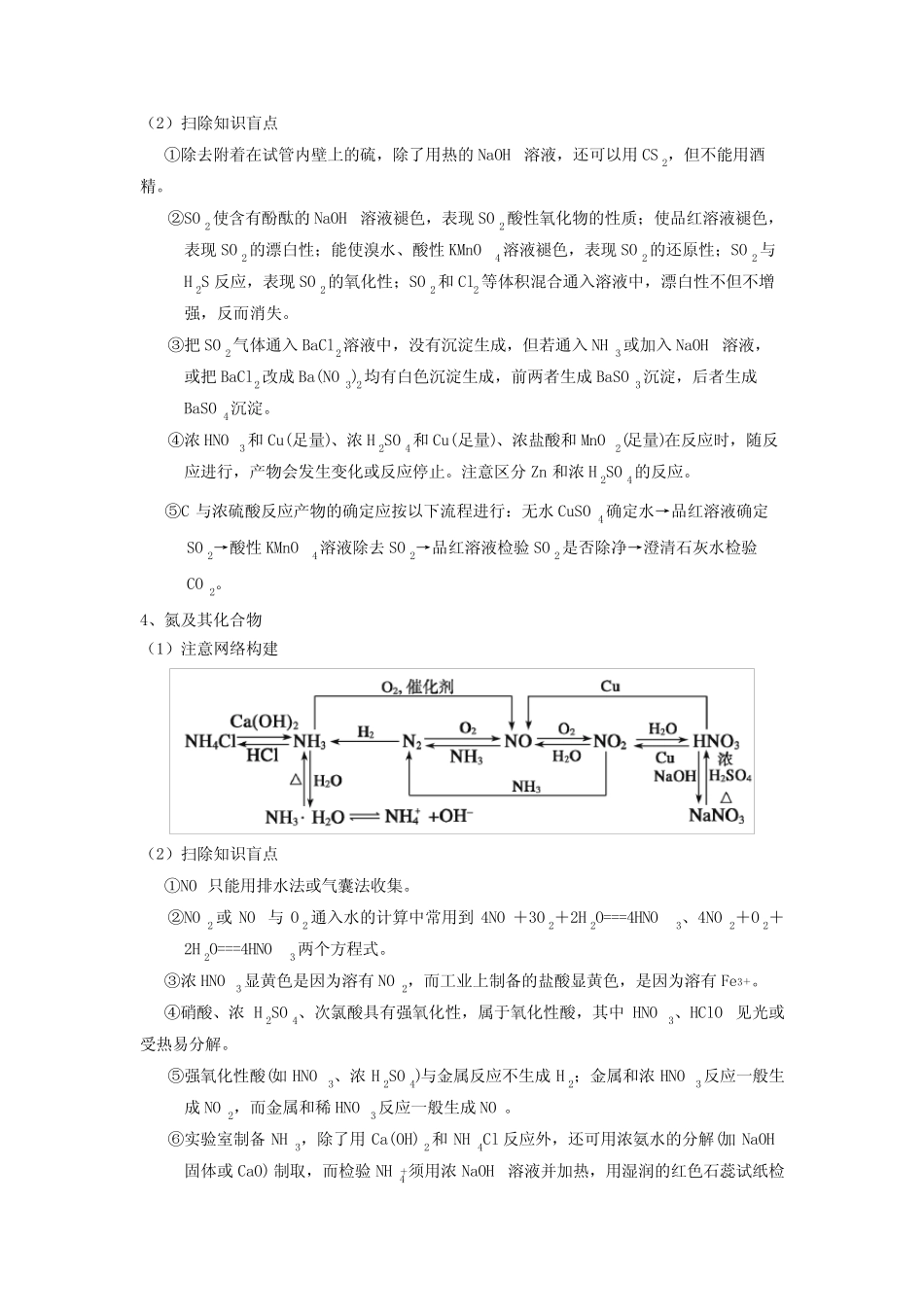
一、知识网络梳理1、碳、硅及其化合物(1)注意网络构建(2)扫除知识盲点①工业上制备粗硅,是用过量的C和SiO2高温下反应,由于C过量,生成的是CO而不是CO2,该反应必须在隔绝空气的条件下进行
②氢氟酸不能用玻璃容器盛放;NaOH溶液能用玻璃试剂瓶,但不能用玻璃塞
③酸性氧化物一般能与水反应生成酸,但SiO2不溶于水;酸性氧化物一般不与酸作用,但SiO2能与HF反应
④硅酸盐大多难溶于水,常见可溶性硅酸盐是硅酸钠,其水溶液称为泡花碱或水玻璃,但却是盐溶液
⑤H2CO3的酸性大于H2SiO3的,所以有Na2SiO3+CO2(少量)+H2O===H2SiO3↓+Na2CO3,但高温下Na2CO3+SiO2=====高温Na2SiO3+CO2↑也能发生,原因可以从两方面解释:①硅酸盐比碳酸盐稳定;②从化学平衡角度,由高沸点难挥发固体SiO2制得低沸点易挥发的CO2
⑥SiO2不导电,是制作光导纤维的材料;Si是半导体,是制作光电池的材料
⑦水泥、玻璃与陶瓷是三大传统无机非金属材料;碳化硅、氮化硅等是新型无机非金属材料
2、氮及其化合物在考查中结合点2、卤素及其重要化合物(1)注意网络构建(2)扫除知识盲点①液氯密封在钢瓶中,而氯水、次氯酸应保存在棕色试剂瓶中
②1molCl2参加反应,转移电子数可能为2NA、NA或小于NA(Cl2和H2O的反应为可逆反应)
③实验室制Cl2,除了用MnO2和浓盐酸反应外,还可以用KMnO4、KClO3、NaClO与浓盐酸反应且都不需要加热,如ClO-+Cl-+2H+===Cl2↑+H2O
④酸性KMnO4溶液,用的是H2SO4酸化而不是盐酸
⑤ClO-不论在酸性环境中还是在碱性环境中均能体现强氧化性,如ClO-与SO2-3、I-、Fe2+均不能大量共存;ClO-体现水解性,因HClO酸性很弱,ClO-水解显碱性,如Fe3++3ClO-+3H2O