配套课时作业时刻:45分钟总分值:100分一、选择题(每题7分,共70分)1.以下既属于氧化还原反映,又属于吸热反映的是()A.铝片与稀盐酸反映B.Ba(OH)2·8H2O与NH4Cl的反映C.灼热的炭与水蒸气的反映D.甲烷(CH4)在O2中的燃烧反映答案C解析铝片与稀盐酸之间的置换反映、甲烷(CH4)在O2中的燃烧反映既是氧化还原反映,又是放热反映;灼热的炭与水蒸气发生的氧化还原反映是吸热反映;Ba(OH)2·8H2O与NH4Cl之间发生的复分解反映是吸热反映,但不是氧化还原反映
2.(2018·郑州市高三质检)以下能量转化进程与氧化还原反映无关的是()A.电解质溶液导电时,电能转化成化学能B.锂离子电池工作时,化学能转化成电能C.硅太阳能电池工作时,光能转化成电能D.葡萄糖为人类生命活动提供能量时,化学能转化成热能答案C解析电解质溶液导电时,电能转化为化学能,发生的反映为氧化还原反映,A项不符合题意;锂离子电池工作时,化学能转化为电能,发生的反映为氧化还原反映,B项不符合题意;硅太阳能电池工作时,光能转化为电能,与氧化还原反映无关,C项符合题意;葡萄糖为人类生命活动提供能量时,葡萄糖发生氧化还原反映,化学能转化为热能,D项不符合题意
3.以下说法不正确的选项是()A.CO2、甲烷都属于温室气体B.用甘蔗生产的燃料乙醇属可再生能源,利用乙醇燃料可不能产生温室气体C.太阳能、风能和生物质能属于新能源D.太阳能电池可将太阳能直接转化为电能答案B解析乙醇作燃料产生CO2气体,会引发温室效应,B项错误
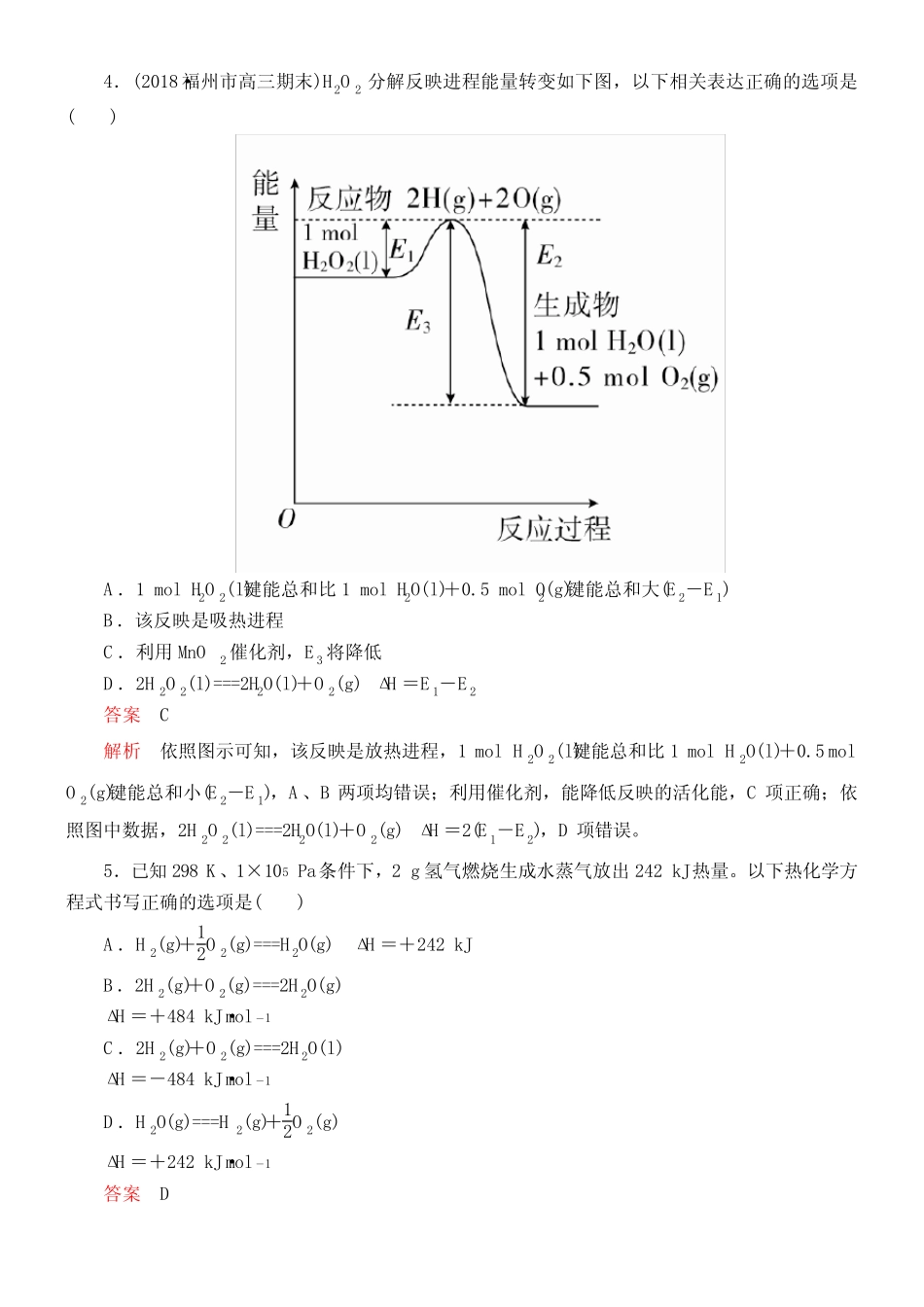
4.(2018·福州市高三期末)H2O2分解反映进程能量转变如下图,以下相关表达正确的选项是()A.1molH2O2(l)键能总和比1molH2O(l)+0
5molO2(g)键能总和大(E2-E1)B.该反映是吸热进程C.利用MnO2催化剂,E3将降低D.2H2O2(l)===2