化学反应与能量的变化(2)【教学目标】1、理解反应热的含义,能判断某反应是吸热还是放热反应
2、能从微观角度,运用化学键的知识,解释化学反应中的能量变化
【教学重点】理解反应热的含义并能进行简单的计算
【教学难点】焓变与反应热的关系的理解
【教学过程】化学反应有质量守恒和能量守恒,能量的多少又直接与质量联系,是以反应物和生成物的质量为基础
一、焓变反应热焓是与内能有关的物理量,反应在一定条件下是吸热还是放热由生成物和反应物的焓值差即焓变(△H)决定
例题1:思考并补齐下图1、反应热:在化学反应过程中所释放或吸收的能量都可以热量(或换成相应的热量)来表示叫反应热,又称“焓变”,符号用△H表示,单位一般采用KJ/mol2、列表讨论放热反应吸热反应表现行式△H﹤0或△H为“—”△H﹥0或△H为“+”能量变化生成物释放的总能量大于反应物吸收的总能量生成物释放的总能量小于反应物吸收的总能量键能变化生成物总键能大于反应物总键能生成物总键能小于反应物总键能联系键能越大,物质能量越低,越稳定,反之键能越小,物质能量越高,越不稳定,3、常见的放热反应有:燃料燃烧酸碱中和等,常见的吸热反应有还原、分解等
4、化学反应的基本特征:化学反应过程中,不仅有物质的变化,还有能量的变化,这种能量的变化常以热能、光能、电能等形式表现出来
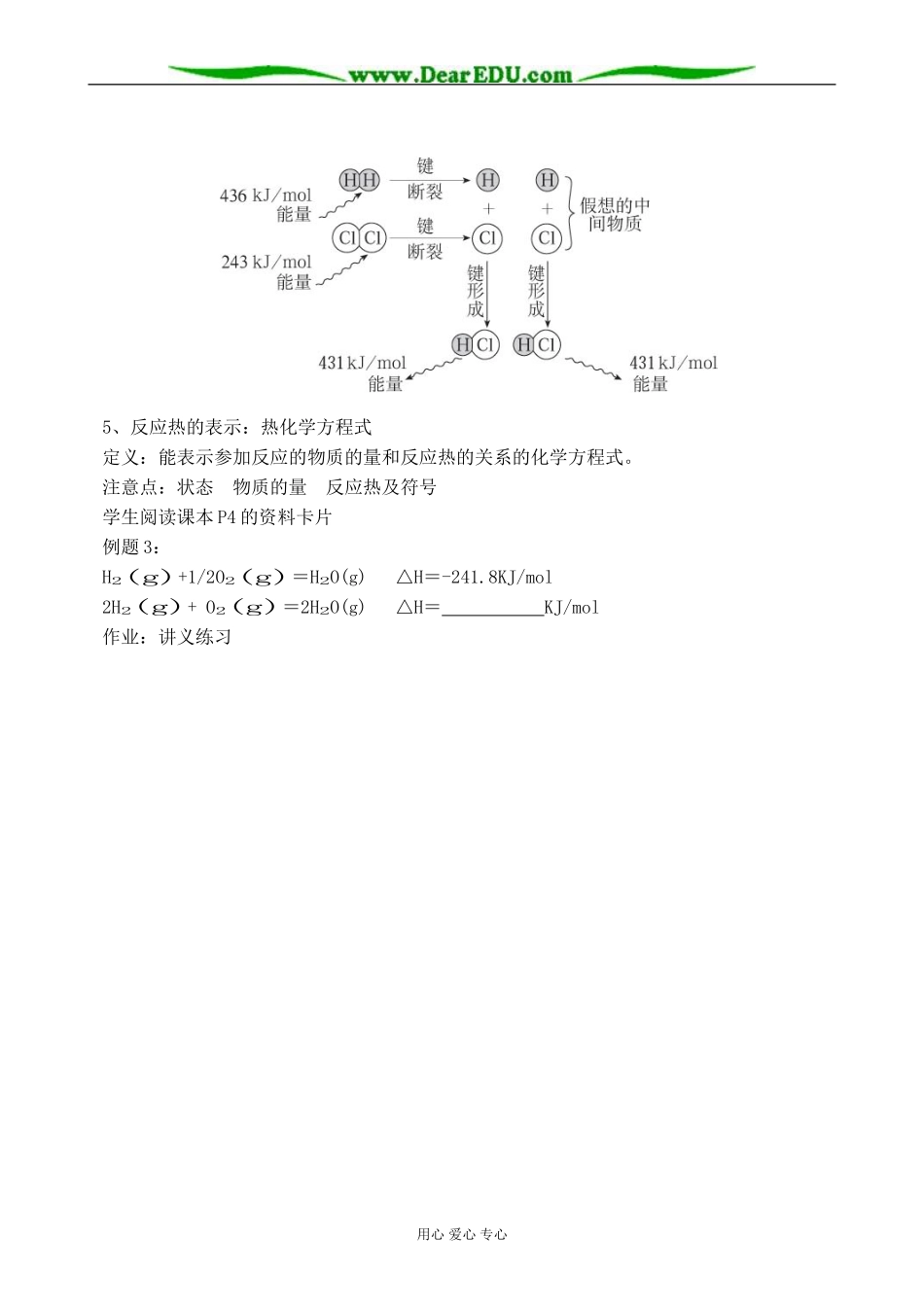
例题2:推导下列变化的反应热△H为多少
用心爱心专心______物能量△H>0______物______反应______物能量△H<0______物______反应5、反应热的表示:热化学方程式定义:能表示参加反应的物质的量和反应热的关系的化学方程式
注意点:状态物质的量反应热及符号学生阅读课本P4的资料卡片例题3:H2(g)+1/2O2(g)=H2O(g)△H=-241
8KJ/mol2H2(g)+O2(g)=2H2O(g)△H=KJ/mol作业:讲义练习用心爱心专心一