苏教版选修三共价键原子晶体教案〖教学目标〗1.认识共价键的本质和特性,了解共价键的饱和性与方向性2.了解共价键的类型3.用电子式法表示共价键的形成过程4.认识影响共价键键能的主要因素,分析化学键的极性强弱,把握键能与化学反应热之间的内在联系5.深化对原子晶体的认识〖课时安排〗4课时第一、二课时〖教学内容〗共价键的形成、共价键的类型【板书】§3-3-1共价键的形成一、定义:原子间通过共用电子对所形成的化学键叫共价键
【设疑】通过共价键的概念我们可以了解形成共价键的粒子是什么呢
为什么要形成共价键
什么元素之间形成共价键
【思考后得出】成键的微粒是原子;成键原子必须有未成对电子,成键后达到稳定结构
一般非金属元素的原子之间可形成共价键
【板书】1、成键微粒:原子
2、成键原因:原子有未成对电子3、成键性质:共用电子对(或电子云重叠)4、成键元素:一般非金属元素(△x<1
7)只含有共价键的化合物称为共价化合物
【设疑】哪些物质中存在共价键
【板书】二、存在共价键的物质(注:书写电子式)(1)非金属单质(除稀有气体外)
如:H2、Cl2、O2、N2等(2)共价化合物
如HCl、H2S、NH3、CH4、CO2(3)某些离子化合物
如NaOH、Ba(OH)2、Na2O2、NH4Cl【过渡】在前一节,我们学习过用电子式表示离子键的形成过程,那么共价键的形成过程如何呢
【板书】三、用电子式表示共价分子的形成过程
【练习】用电子式表示H2、HCl、Cl2分子的形成过程
【设问】两个氢原子之间一定能形成稳定的共价键吗
39【总结】只有两个自旋方向相反的未成对电子才能形成稳定的共价键
【设问】为什么没有He2、H3、H2Cl、Cl3分子【阅读】p
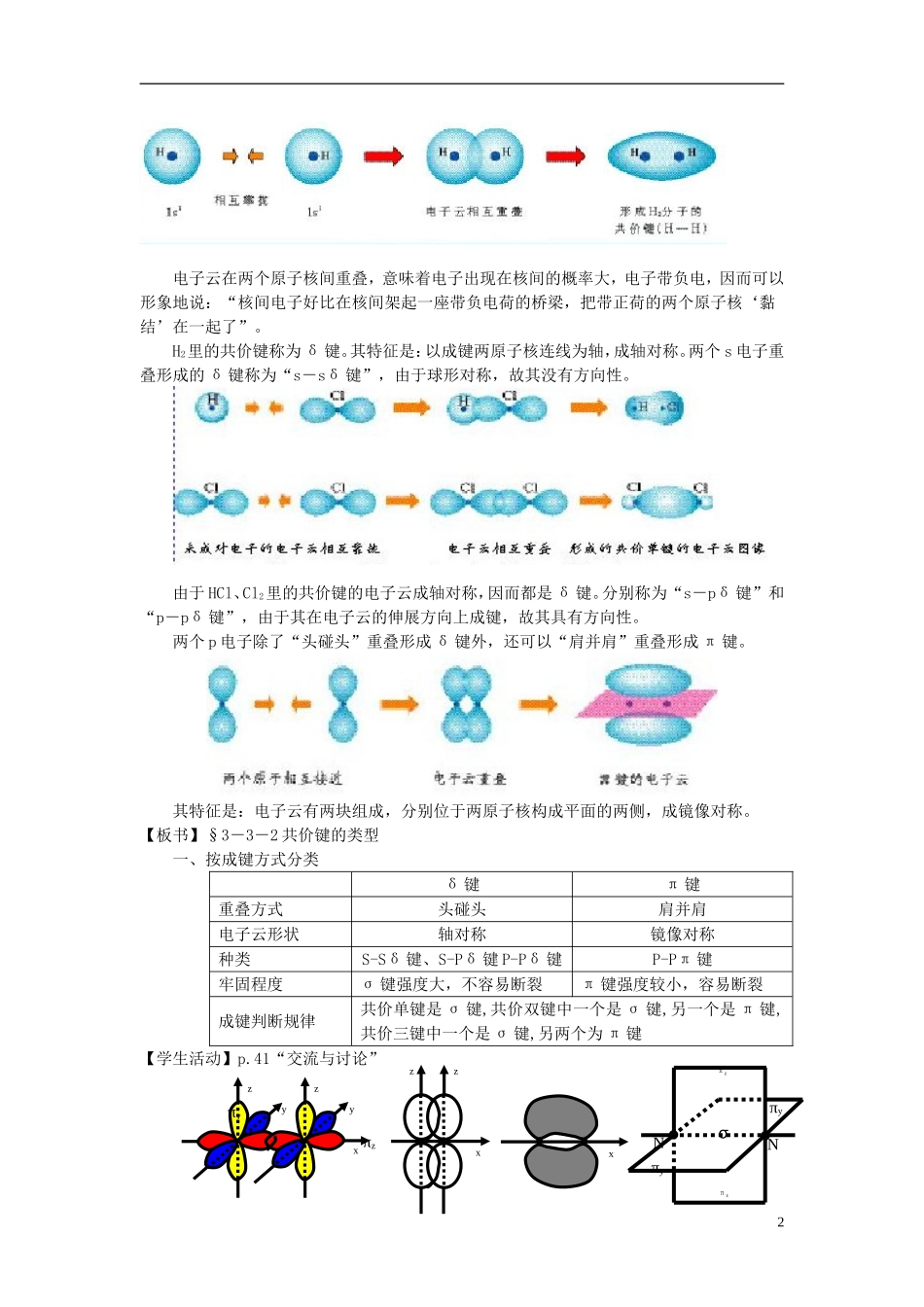
40【板书】四、共价键的特点1.具有饱和性:形成的共价键数=未成对电子数【讲解】用电子云描述氢分子的形成1电子云在两个原子核间重叠,意味