第二节分子的立体结构第一课时教学目标:1
了解一些典型分子的立体结构,认识分子结构的多样性和复杂性,理解价层电子对互斥模型
通过对典型分子立体结构探究过程,学会运用观察、比较、分类及归纳等方法对信息进行加工,提高科学探究能力
通过PowerPoint展示分子的立体结构,激发学习化学的兴趣,感受化学世界的奇妙
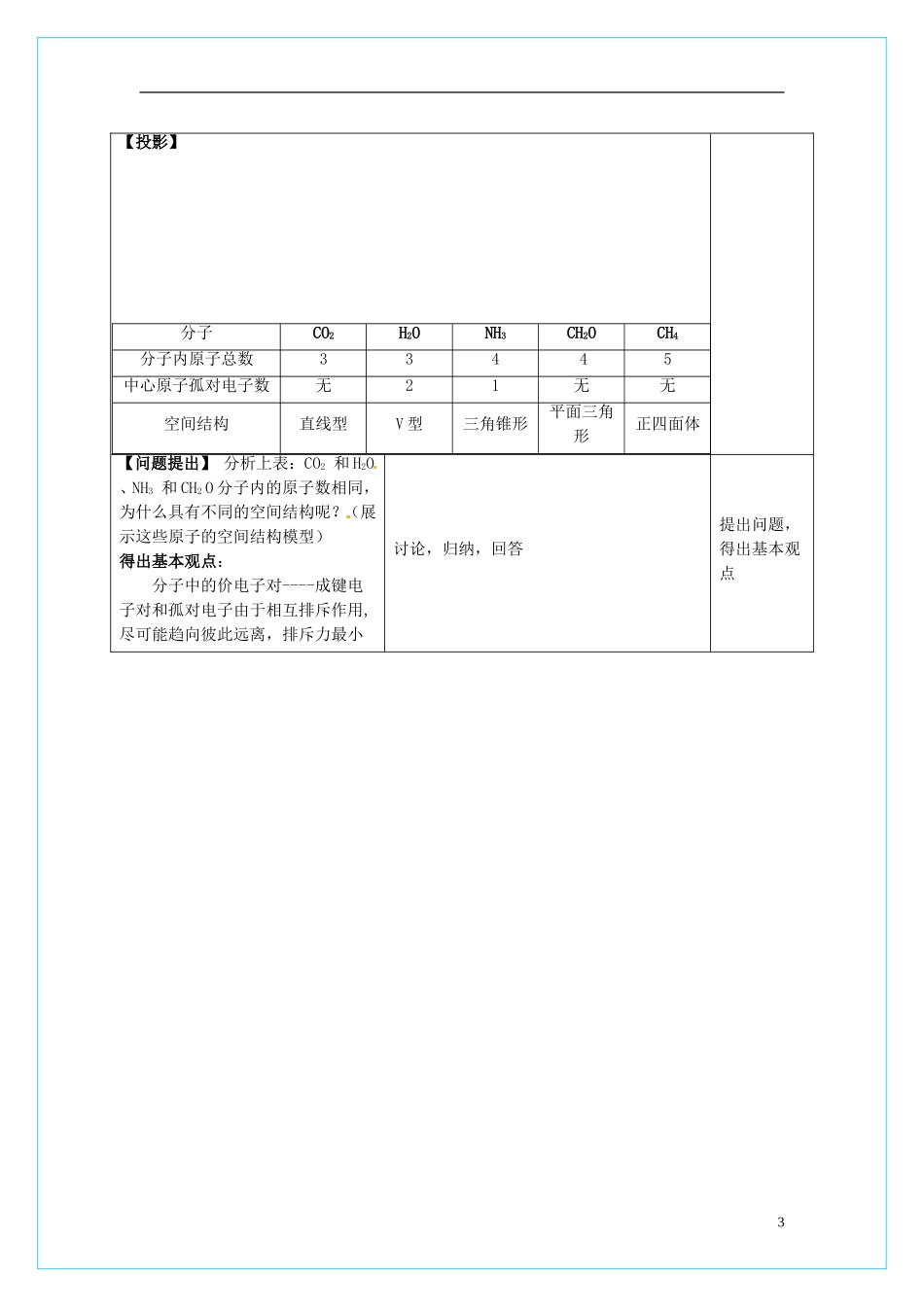
教学重点:价层电子对互斥模型教学难点:能用价层电子对互斥模型解释分子的立体结构教学方法:分组讨论,启发式、多媒体辅助教学教学过程:教师活动学生活动设计意图【投影】展示CO2、H2O、NH3、CH2O、CH4等分子的球辊模型(或比例模型)阅读课本P37-40内容;观察一些典型分子的立体结构,观察,分析
让学生对分子的空间结构有直观的认识【板书】2
1形形式式的分子【提出问题】什么是分子的空间结构
结构式能反映出分子的空间构造吗
讨论分子在三维空间的构造情况
让学生区分结构式与空间结构的区别【归纳】结构式不能反映出分子的空间结构【思考】1
同为三原子分子,CO2和H2O分子的空间结构却不同,什么原因
同为四原子分子,CH2O与NH3分子的的空间结构也不同,什么原因
记忆【黑板练习】写出C、H、N、O的电子式,根据共价键的饱和性讨论C、H、N、O的成键情况
原子HCNO电子式可形成共用电子对数1432成键情况1432复习旧知识,培养学生知识归纳的能力1【归纳】原子不同,可形成的电子对数目不同,共价键的饱和性不同【黑板练习】写出CO2、H2O、NH3、CH2O、CH4的电子式和结构式;根据电子式、结构式描述CO2、H2O、NH3、CH2O、CH4的成键情况
分析分子内的原子总数、孤对电子数及空间结构
分子CO2H2ONH3CH2OCH4电子式结构式O=C=OH-O-H原子总数33445孤对电子数无21无无空间结构直线型V型三角锥形平面三角形正四面体发挥学