溶液的配制及分析【教学目标】初步学会配制一定物质的量浓度溶液的实验技能
【教学重点】配制一定物质的量浓度溶液的实验技能【教学难点】定物质的量浓度溶液的实验分析【教学过程】一、物质的量浓度1.定义:单位体积溶液中所含溶质B的物质的量
2.公式:CB=n/v,溶液的体积、溶质的物质的量
〖问题解决〗学生完成二、溶液的配制1.容量瓶的使用:(1)容量瓶:是准确配制一定体积、一定浓度溶液的仪器
(2)组成:瓶体和瓶塞两部分
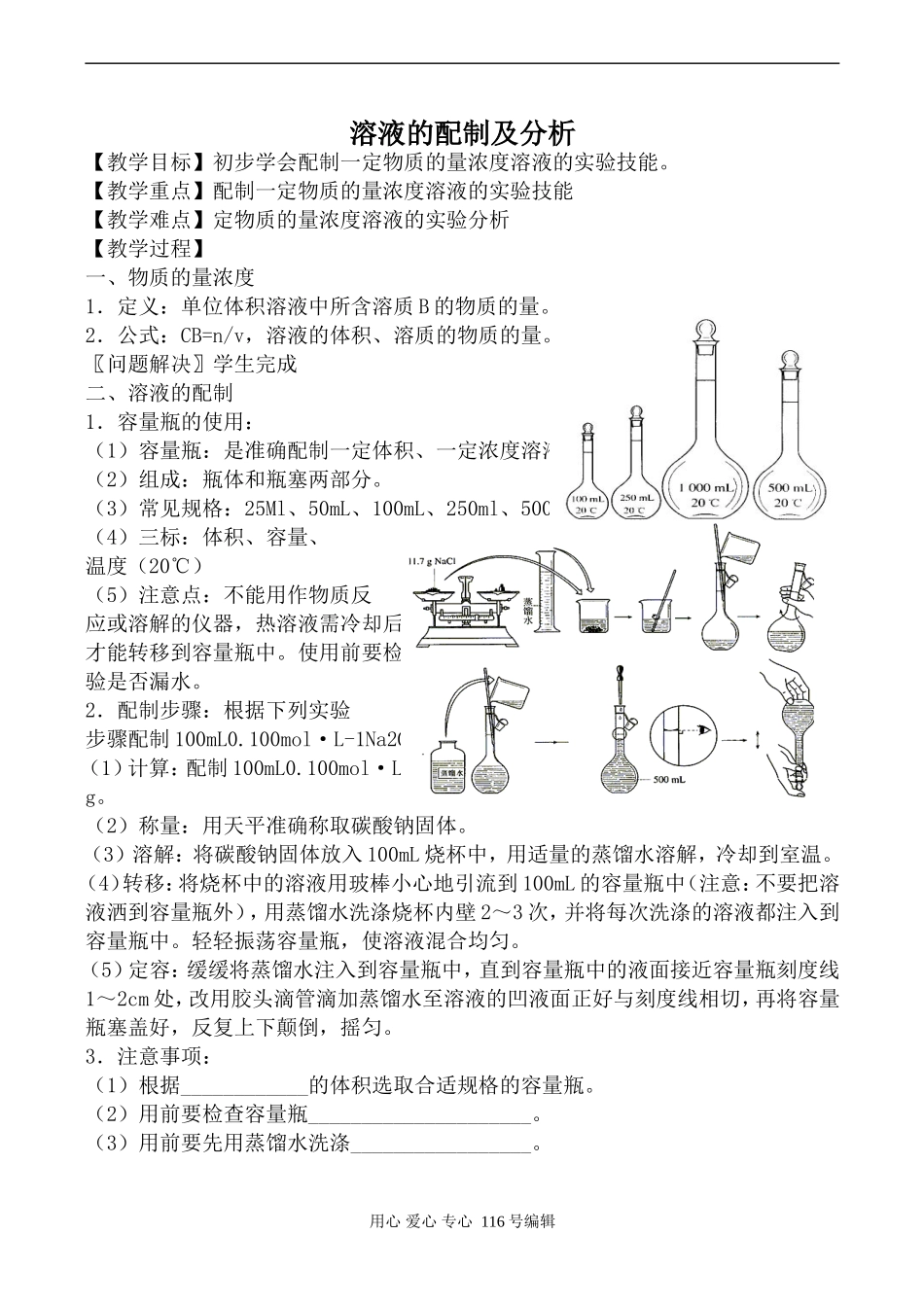
(3)常见规格:25Ml、50mL、100mL、250ml、500ml、1000mL
(4)三标:体积、容量、温度(20℃)(5)注意点:不能用作物质反应或溶解的仪器,热溶液需冷却后才能转移到容量瓶中
使用前要检验是否漏水
2.配制步骤:根据下列实验步骤配制100mL0
100mol·L-1Na2CO3溶液
(1)计算:配制100mL0
100mol·L—1Na2CO3溶液所需Na2CO3固体的质量为g
(2)称量:用天平准确称取碳酸钠固体
(3)溶解:将碳酸钠固体放入100mL烧杯中,用适量的蒸馏水溶解,冷却到室温
(4)转移:将烧杯中的溶液用玻棒小心地引流到100mL的容量瓶中(注意:不要把溶液洒到容量瓶外),用蒸馏水洗涤烧杯内壁2~3次,并将每次洗涤的溶液都注入到容量瓶中
轻轻振荡容量瓶,使溶液混合均匀
(5)定容:缓缓将蒸馏水注入到容量瓶中,直到容量瓶中的液面接近容量瓶刻度线1~2cm处,改用胶头滴管滴加蒸馏水至溶液的凹液面正好与刻度线相切,再将容量瓶塞盖好,反复上下颠倒,摇匀
3.注意事项:(1)根据____________的体积选取合适规格的容量瓶
(2)用前要检查容量瓶_____________________
(3)用前要先用蒸馏水洗涤_________________
用心爱心专心116号编辑(4)容量瓶中不能直接溶解或稀释固体或浓溶液,也不能