教学时间第十周4月23日本模块第26课时教学课题专题专题2化学反应速率与化学平衡单元第三单元化学平衡的移动节题第五课时温度对平衡浓度的影响教学目标知识与技能通过浓度、压强、温度对化学平衡的影响,并能用相关理论加以解释
过程与方法根据化学反应速率、化学平衡移动理论分析合成氨工业
情感态度与价值观通过对合成氨工业的实际影响,体会化学反应在生活、生活中的实际应用
教学重点合成氨的适宜条件教学难点化学平衡移动原理的实际应用
教学方法讨论法、探究法教学过程教师主导活动学生主体活动[提问]化学平衡移动原理的内容
1.原料气的制备、净化①制N2:物理方法:空气液态空气N2化学方法:空气CO2+N2N2②制H2:水蒸气CO+H2CO2+H2H2反应方程式为:C+H2O(g)==CO+H2;CO+H2O(g)==CO2+H2注意:制得的N2、H2需要净化,清除杂质,以防止催化剂“中毒”
合成氨反应的特点化学反应:N2+3H22NH3△H=-92
4KJ(1)可逆反应;(2)正反应是放热反应;(3)正反应是气体体积缩小的反应
用心爱心专心1压缩蒸发炭赤热炭H2O催化剂(去CO2)燃烧(去CO2)△教学过程教师主导活动学生主体活动3.工业合成氨适宜条件的选择在实际生产中,需要考虑反应速率、化学平衡、原料选择、产量和设备等多方面情况,以确定最佳的生产条件
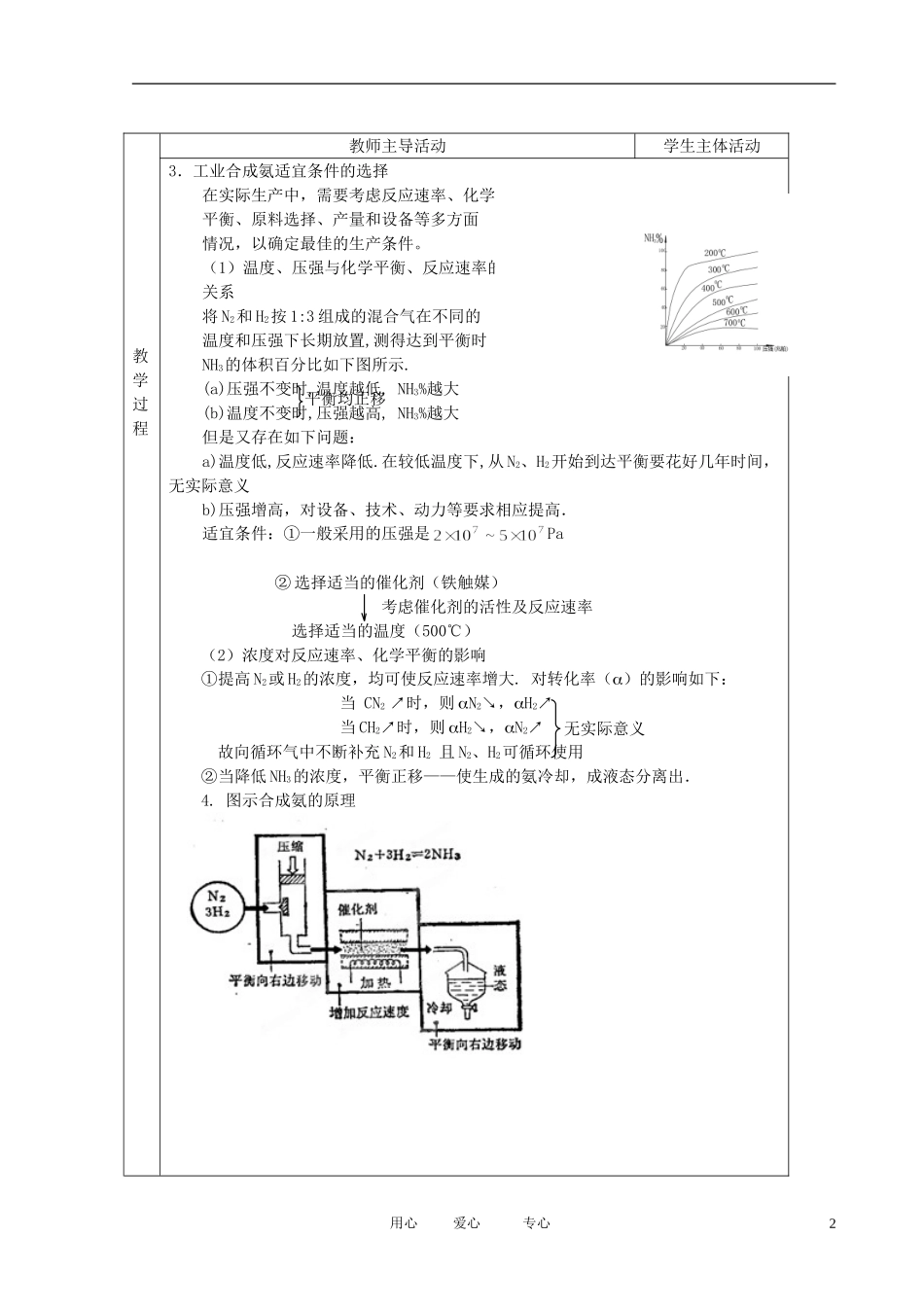
(1)温度、压强与化学平衡、反应速率的关系将N2和H2按1:3组成的混合气在不同的温度和压强下长期放置,测得达到平衡时NH3的体积百分比如下图所示
(a)压强不变时,温度越低,NH3%越大(b)温度不变时,压强越高,NH3%越大但是又存在如下问题:a)温度低,反应速率降低
在较低温度下,从N2、H2开始到达平衡要花好几年时间,无实际意义b)压强增高,对设备、技术、动力等要求相应提高.适宜条件:①一般采用的压强是Pa②选择适当的催化剂(铁触媒)