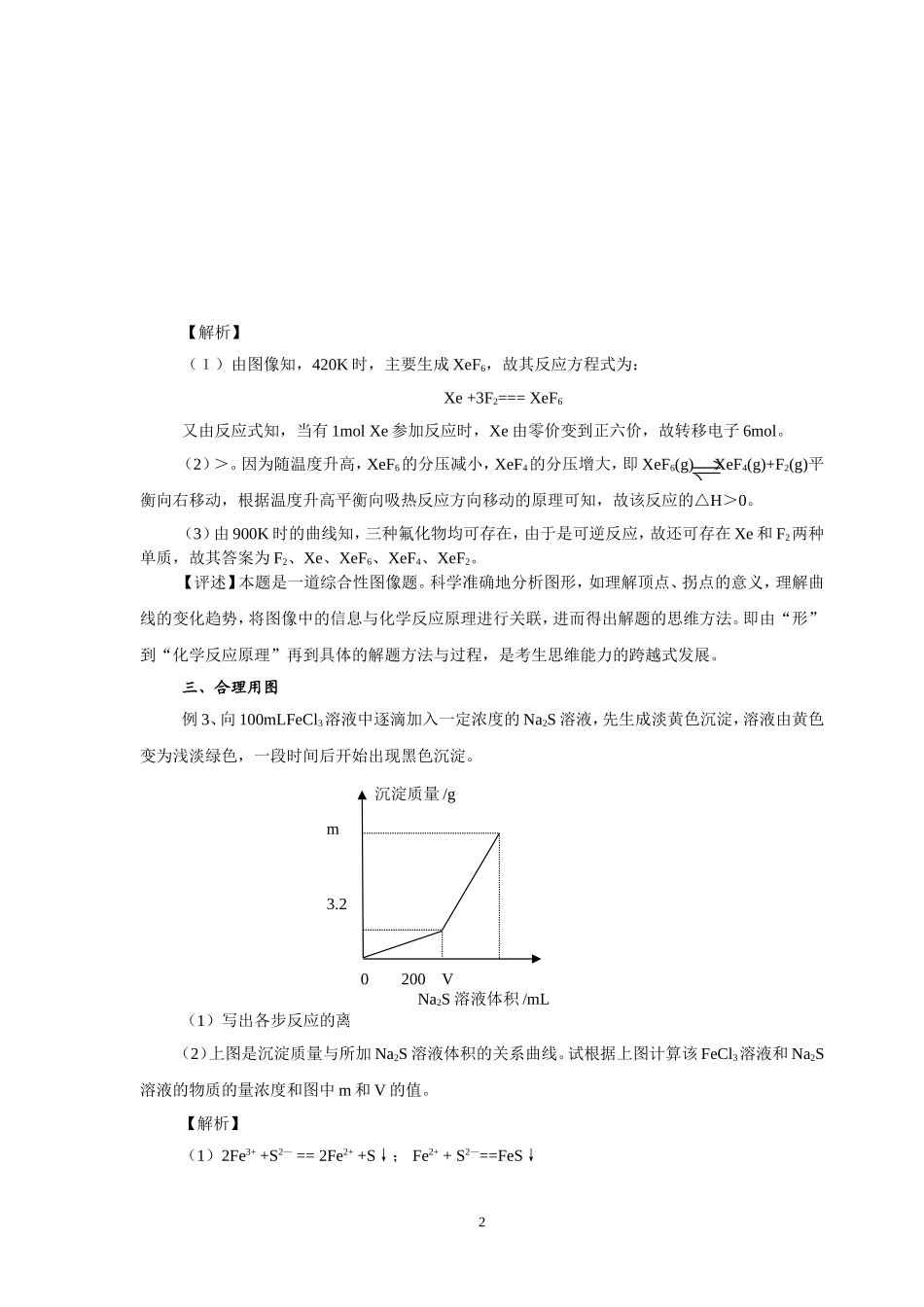
化学图像题的优化解法深圳市宝安区教育局教研室(广东深圳518101)左香华化学图像题具有简明、直观等特点,它是“化学反应原理”与“数”和“形”的有机统一。解答化学图像题的基础是化学反应原理,将化学反应中的定量关系以“数”的形式进行呈现,进而作图,便得到一种“形”的升华。如何解答这一类化学试题,是本文研究的重点问题。一、正确识图例1、(05年广东省高考化学试题14)在一定条件下,固定容积的密闭容器中反应:2NO2(g)O2(g)+2NO(g);△H>0,达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是A、当X表示温度时,Y表示NO2的物质的量B、当X表示压强时,Y表示NO2的转化率C、当X表示反应时间时,Y表示混合气体的密度D、当X表示NO2的物质的量时,Y表示O2的物质的量【解析】由图可知,Y随X的增大而逐渐减小,而该反应的特点是正反应是一体积增大的吸热反应。当升高温度时(X增大),平衡向正反应方向移动,NO2的物质的量减少;当增大压强时(X增大),平衡向逆反应方向移动,NO2的转化率减小。而在一个固定容积的密闭容器中,混合气体的密度是不随时间的变化而发生改变的;当增大NO2的物质的量时,平衡正向移动,O2的物质的量增多。因此答案为AB。【评述】坐标轴的意义与化学反应原理的对应实质上是考生对化学反应原理的形象化认识。明确化学反应原理是解答这一类试题的基础,正确识图是解答这一类试题的关键。本题使用勒沙特列原理结合图像进行分析便可作答。二、科学析图例2、(05年广东省高考化学试题23)在密闭容器中,由一定起始浓度的氙(Xe)和F2反应,可得到3种氟化物。各种生成物在平衡体系内的分压与反应温度的关系如下图所示(已知气体的分压之比等于物质的量之比)。(1)420K时,发生反应的化学方程式为:;若反应中消耗1molXe,则则转移电子mol。(2)600~800K时,会发生反应XeF6(g)XeF4(g)+F2(g)其反应热△H0(填“>”、“=”或“<”)(3)900K时,容器中存在的组分有。1XY平衡体系的分压/kPa1002003004005006007008003404005006007008009001000XeF4XeF2XeF6温度/K【解析】(1)由图像知,420K时,主要生成XeF6,故其反应方程式为:Xe+3F2===XeF6又由反应式知,当有1molXe参加反应时,Xe由零价变到正六价,故转移电子6mol。(2)>。因为随温度升高,XeF6的分压减小,XeF4的分压增大,即XeF6(g)XeF4(g)+F2(g)平衡向右移动,根据温度升高平衡向吸热反应方向移动的原理可知,故该反应的△H>0。(3)由900K时的曲线知,三种氟化物均可存在,由于是可逆反应,故还可存在Xe和F2两种单质,故其答案为F2、Xe、XeF6、XeF4、XeF2。【评述】本题是一道综合性图像题。科学准确地分析图形,如理解顶点、拐点的意义,理解曲线的变化趋势,将图像中的信息与化学反应原理进行关联,进而得出解题的思维方法。即由“形”到“化学反应原理”再到具体的解题方法与过程,是考生思维能力的跨越式发展。三、合理用图例3、向100mLFeCl3溶液中逐滴加入一定浓度的Na2S溶液,先生成淡黄色沉淀,溶液由黄色变为浅淡绿色,一段时间后开始出现黑色沉淀。(1)写出各步反应的离子方程式。(2)上图是沉淀质量与所加Na2S溶液体积的关系曲线。试根据上图计算该FeCl3溶液和Na2S溶液的物质的量浓度和图中m和V的值。【解析】(1)2Fe3++S2—==2Fe2++S↓;Fe2++S2—==FeS↓2沉淀质量/gm3.20200VNa2S溶液体积/mL(2)由图知:n(S)===3.2g/32g·mol—1===0.1mol2Fe3++S2—==2Fe2++S↓0.2mol0.1mol0.2mol0.1molc(Na2S)===0.1mol/0.2L==0.5mol/Lc(FeCl3)===0.2mol/0.1L==2mol/Lm==0.2mol88g/mol+3.2g==20.8g(V-200)10-3L×0.5mol/L===0.2molV==0.6L==600mL四、细心作图例4、已知Fe2O3在高炉中有下列反应:Fe2O3+CO2FeO+CO2反应形成的固体混合物(Fe2O3、FeO)中,元素铁和氧的质量比用mFe︰mO表示。(1)上述固体混合物中,mFe︰mO不可能是(选填a、b、c,多选扣分)(a)21︰9(b)21︰7.5(c)21︰6(2)若mFe︰mO==21︰8,计算Fe2O3被CO还原的百分率。(3)设Fe2O3被CO还原的百分率为A%,则A%和混合物中mFe:mO的关系式为(用含mFe、mO的代数式表示)。A%==请在右图中画出A%...