高一化学反应速率基础知识练习题一、单选题1
下列关于化学反应速率的说法,不正确的是()A
化学反应速率是衡量化学反应进行快慢程度的物理量B
单位时间内某物质的浓度变化大,则该物质反应就快C
化学反应速率可以用单位时间内生成某物质的质量的多少来表示D
化学反应速率常用单位有molL1s1和molL1min12
在N2+3H22NH3反应中,自反应开始至2s末,氨的浓度由0变为0
4mol·L-1,则以氢气的浓度变化表示该反应在2s内的平均反应速率是()A
3mol·L-1·s-1B
4mol·L-1·s-1C
6mol·L-1·s-1D
8mol·L-1·s-13
实验室常用H2O2溶液分解制取O2,下列措施可使反应速率减慢的是()A
加入MnO2B
用冰水冷却C
增大H2O2溶液浓度D
溶液适当加热4
反应A+3B=2C+D在四种不同情况下的反应速率分别为①v(A)=0
15mol·L-1·s-1,②v(B)=0
6mol·L-1·s-1,③v(C)=0
5mol·L-1·s-1,④v(D)=0
45mol·L-1·s-1
则反应进行的快慢顺序为()A
④>③>①>②B
②>④>③>①C
②>③>④>①D
④>③>②>①5
已知反应2NOg2H2gƒN2g2H2Og△H752kJmol-1的反应机理如下:①2NOgƒN2O2g快②N2O2gH2g==N2OgH2Og慢③N2OgH2g==N2gH2Og快下列有关说法正确的是()A
N2O2和N2O是该反应的催化剂B
②的反应的活化能最小C
反应速率vNO=vH2=vN2D
总反应中逆反应的活化能比正反应的活化能大6
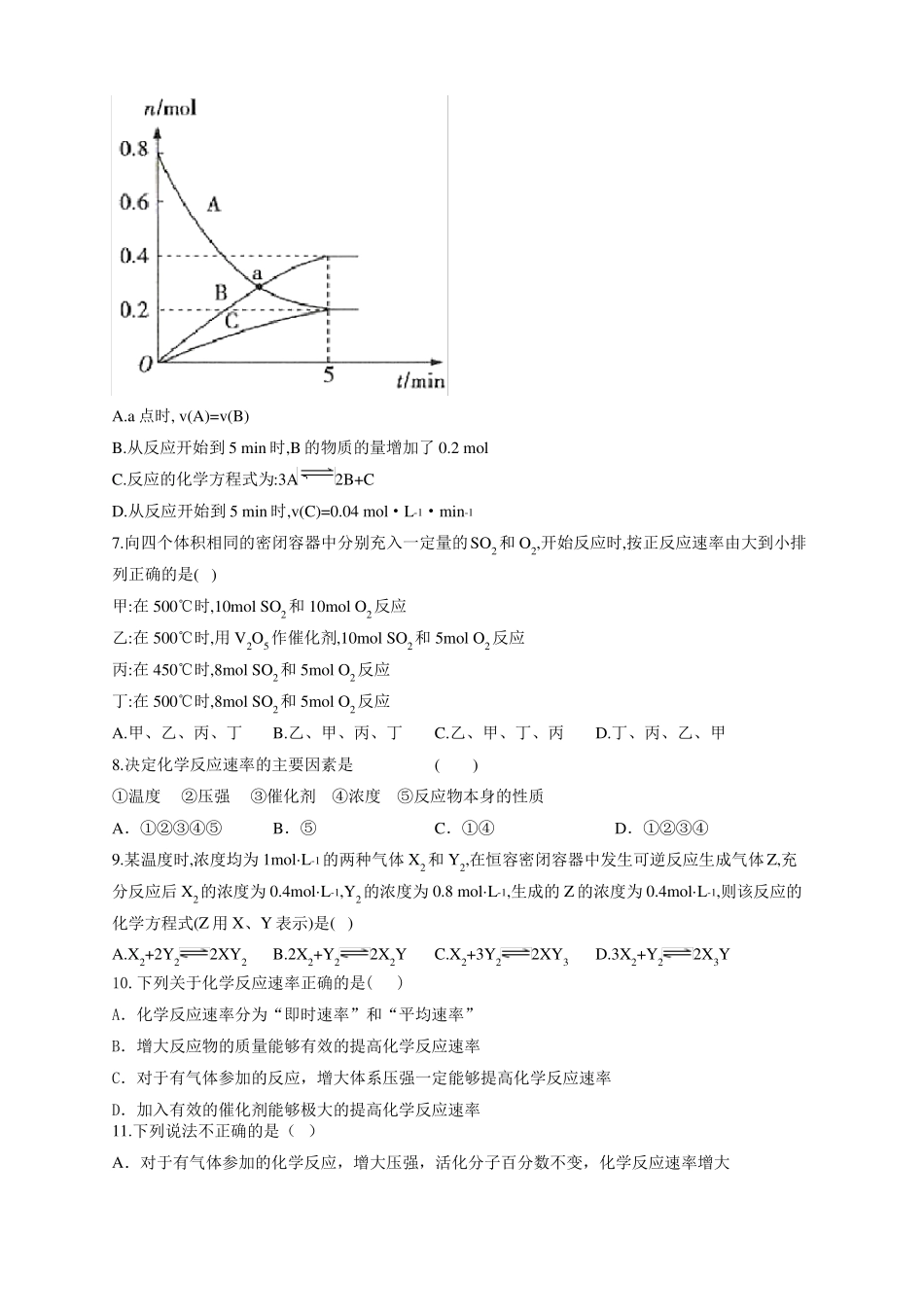
一定温度下,在2L恒容密闭容器中,A、B、C三种气体的物质的量随时间变化的曲线如图