第一节原电池一、教学目标进进一步了解原电池的工作原理,能够写出电极反应式和总反应方程式
二、教学重点认识原电池概念、原理、组成及应用
三、教学难点原电池的工作原理,引导学生从电子转移角度理解化学能向电能转化的本质
四、教学过程【引入】播放相关录像,帮助学生形成感性认识
【板书】第一节原电池一、原电池实验探究讲:铜片、锌片、硫酸都是同学们很熟悉的物质,利用这三种物质我们再现了1799年意大利物理学家----伏打留给我们的历史闪光点
【实验探究】(铜锌原电池)×实验步骤1、锌片插入稀硫酸2、铜片插入稀硫酸现象CuZn3、锌片和铜片上端连接在一起插入稀硫酸【问题探究】1、锌片和铜片分别插入稀硫酸中有什么现象发生
2、锌片和铜片用导线连接后插入稀硫酸中,现象又怎样
3、锌片的质量有无变化
溶液中c(H+)如何变化
4、锌片和铜片上变化的反应式怎样书写
5、电子流动的方向如何
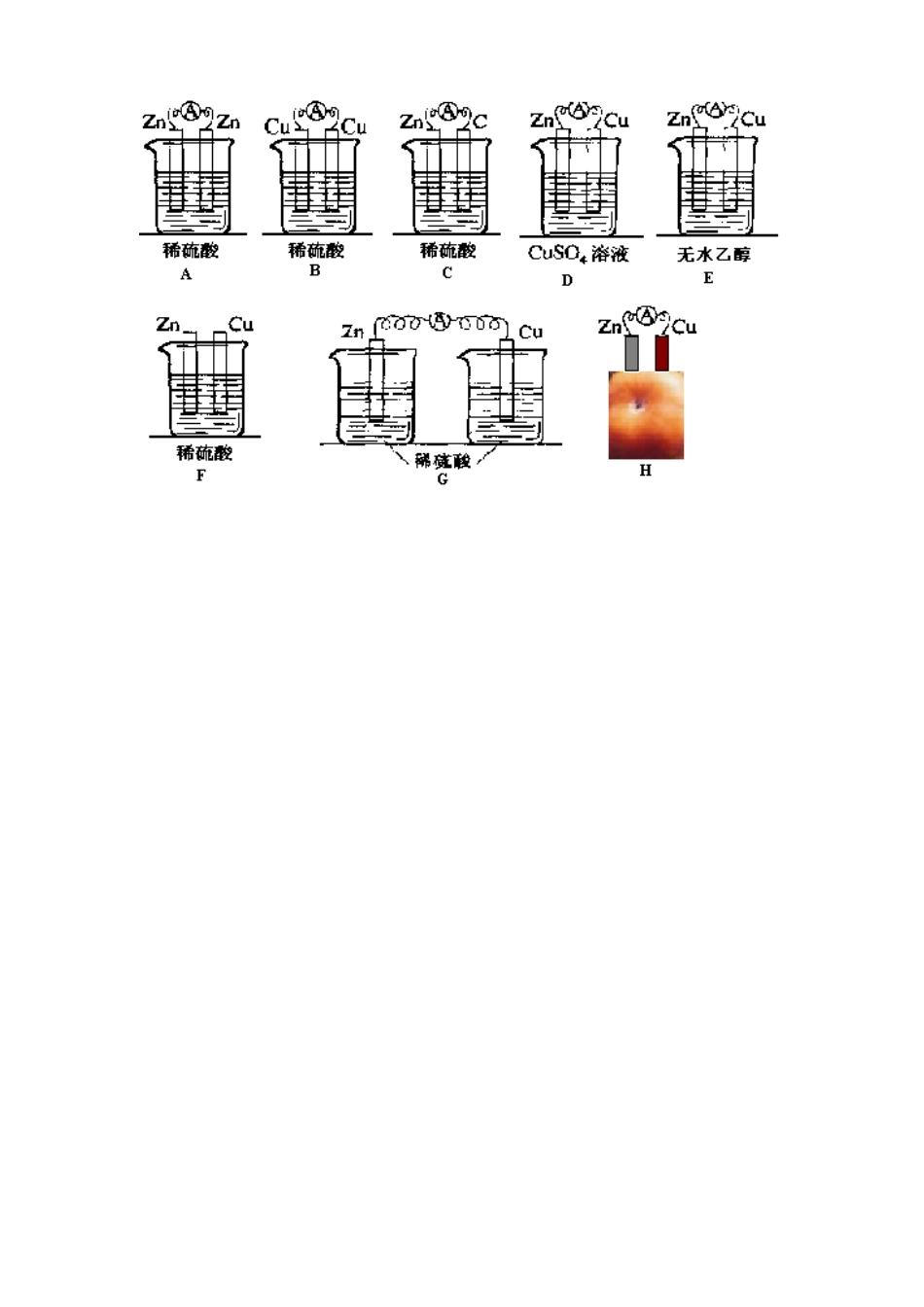
二、原电池的构成条件1、两个电极2、电解质溶液3、形成闭合回路(导线连接或直接接触且电极插入电解质溶液4、自发的氧化还原反应思考:如何根据氧化还原反应原理来设计原电池呢
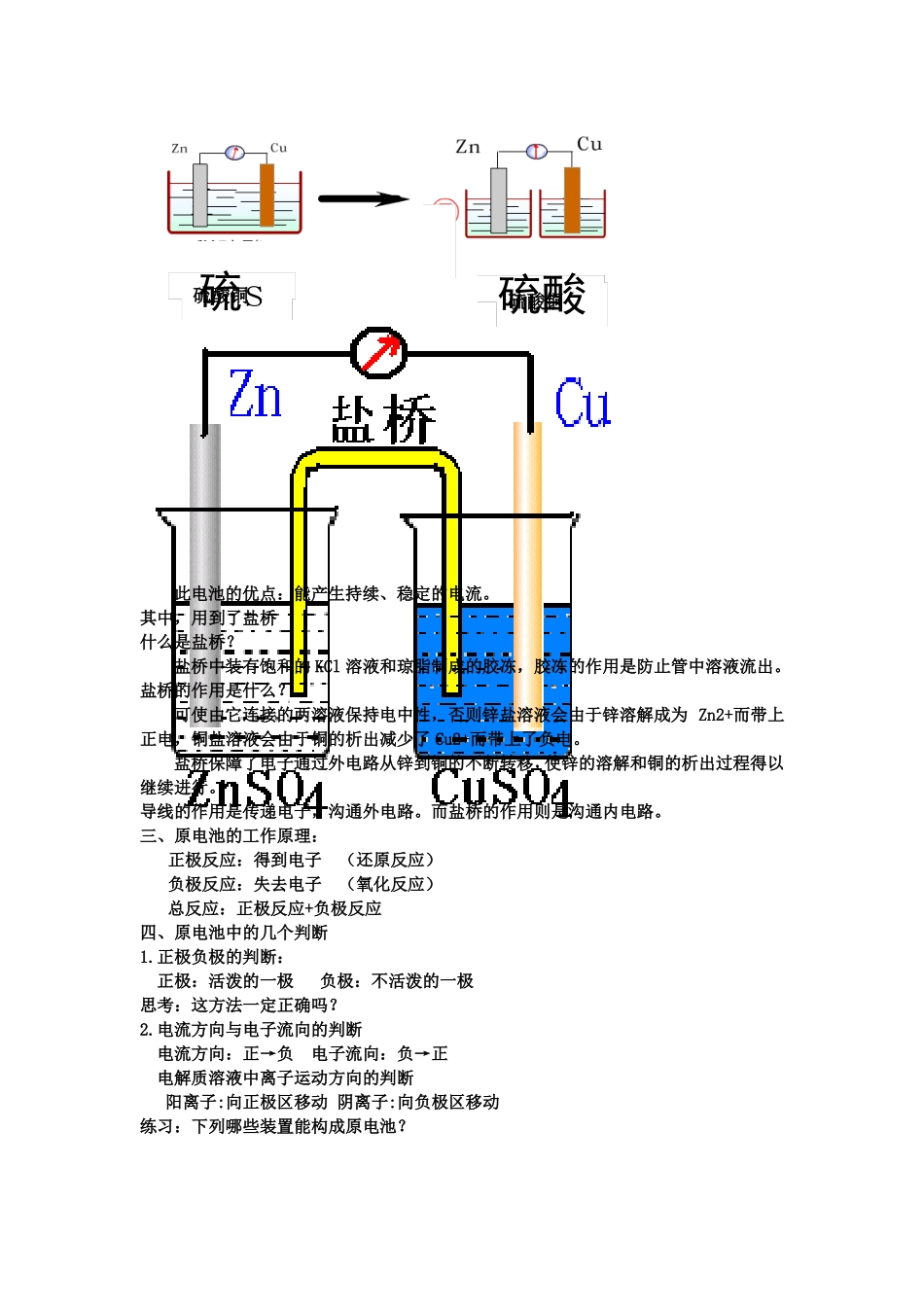
请将氧化还原反应Zn+Cu2+=Cu+Zn2+设计成电池:硫酸铜硫s硫酸硫酸铜此电池的优点:能产生持续、稳定的电流
其中,用到了盐桥什么是盐桥
盐桥中装有饱和的KCl溶液和琼脂制成的胶冻,胶冻的作用是防止管中溶液流出
盐桥的作用是什么
可使由它连接的两溶液保持电中性,否则锌盐溶液会由于锌溶解成为Zn2+而带上正电,铜盐溶液会由于铜的析出减少了Cu2+而带上了负电
盐桥保障了电子通过外电路从锌到铜的不断转移,使锌的溶解和铜的析出过程得以继续进行
导线的作用是传递电子,沟通外电路
而盐桥的作用则是沟通内电路
三、原电池的工作原理:正极反应:得到电子(还原反应)负极反应:失去电子(氧化反应)总反应:正极反应+负极反应四、原电池中的几个判断1