侯式制碱法原理和简单流程知识精讲【知识梳理】实验背景:无水碳酸钠,俗名纯碱、苏打
它是玻璃、造纸、肥皂、洗涤剂、纺织、制革等工业的重要原料,还常用作硬水的软化剂,也用于制造钠的化合物
它的工业制法主要有氨碱法和联合制碱法两种
一、实验原理化学反应原理是:总反应为:将经过滤、洗涤得到的NaHCO3微小晶体再加热,制得纯碱产品:答案:化学反应原理:NH3CO2H2ONH4HCO3NaCl(饱和)NH4HCO3NaHCO3NH4Cl总反应:NaCl(饱和)NH3CO2H2ONaHCO3NH4Cl2NaHCO3Na2CO3CO2H2O二、氨碱法(又称索尔维法)1.原料:食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气2.步骤:先把氨气通入饱和食盐水中而成氨盐水,NH3CO2H2ONH4HCO3再通入二氧化碳生成溶解度较小的碳酸氢钠沉淀和氯化铵溶液,NaCl(饱和)NH4HCO3NaHCO3NH4Cl将经过滤、洗涤得到的NaHCO3微小晶体,再加热煅烧制得纯碱产品
2NaHCO3Na2CO3CO2H2O(放出的二氧化碳气体可回收循环使用)含有氯化铵的滤液与石灰乳[Ca(OH)2]混合加热,所放出的氨气可回收循环使用
CaO+H2OCa(OH)2,2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O其工业流程图为:1
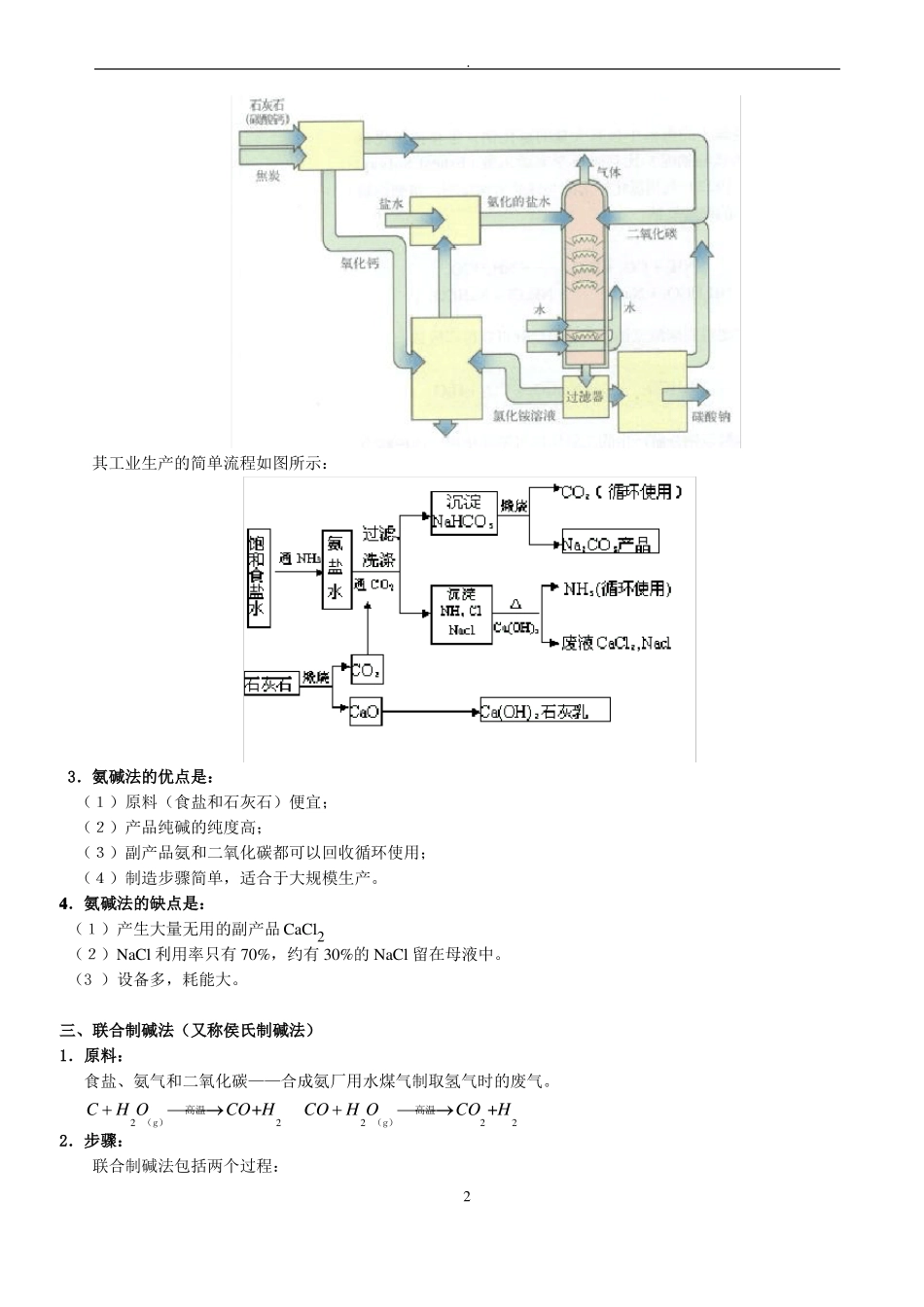
其工业生产的简单流程如图所示:3.氨碱法的优点是:(1)原料(食盐和石灰石)便宜;(2)产品纯碱的纯度高;(3)副产品氨和二氧化碳都可以回收循环使用;(4)制造步骤简单,适合于大规模生产
4.氨碱法的缺点是:(1)产生大量无用的副产品CaCl2(2)NaCl利用率只有70%,约有30%的NaCl留在母液中
(3)设备多,耗能大
三、联合制碱法(又称侯氏制碱法)1.原料:食盐、氨气和