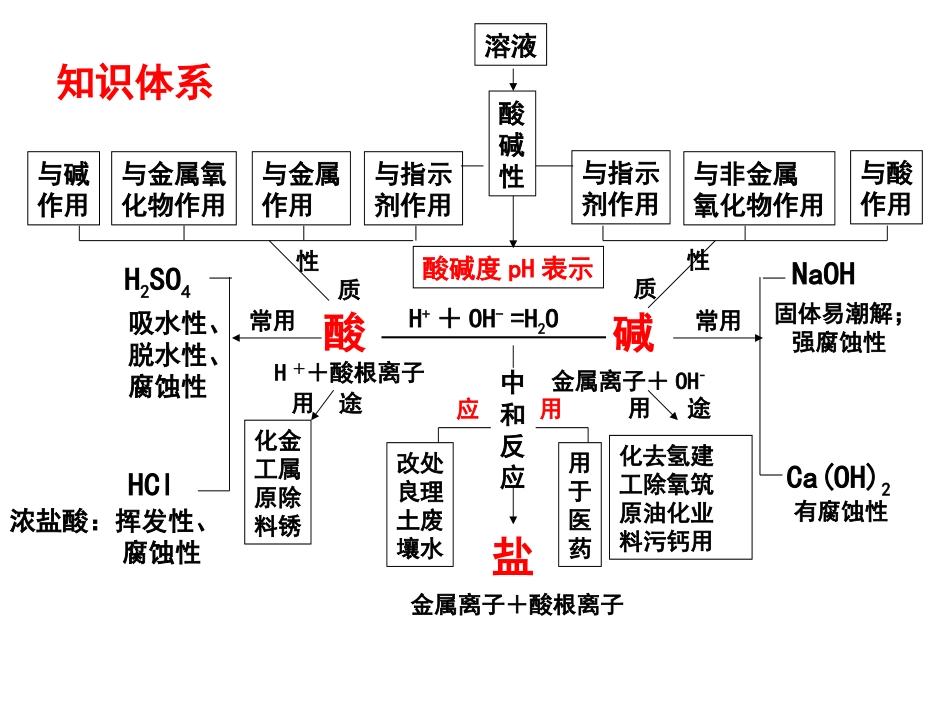
酸和碱复习课第十单元酸和碱复习课3、掌握酸的通性、碱的通性、酸碱中和反应及其应用1、掌握盐酸、硫酸的物理性质和化学性质2、掌握氢氧化钠、氢氧化钙物理性质和化学性质吸水性、脱水性、腐蚀性知识体系固体易潮解;强腐蚀性溶液H++酸根离子Ca(OH)2H2SO4HCl常用浓盐酸:挥发性、腐蚀性与金属氧化物作用与酸作用与金属作用与碱作用性质化金工属原除料锈用途酸碱金属离子+OH-盐中和反应金属离子+酸根离子H++OH-=H2ONaOH常用与指示剂作用与指示剂作用与非金属氧化物作用性质酸碱性酸碱度pH表示化去氢建工除氧筑原油化业料污钙用应用用途改处良理土废壤水用于医药有腐蚀性一、常见的酸和碱1
常见的酸有_____________________________相应化学式为_______________________常见的碱有_________________相应化学式________________________________盐酸、硫酸、碳酸、醋酸等氢氧化钠、氢氧化钙、氢氧化钾、氨水等HClH2SO4H2CO3CH3COOHNaOHCa(OH)2KOHNH3
H2O纯净的硫酸是____色液体,不易挥发,易溶于水,溶解时
浓硫酸有性,所以可作干燥剂,浓硫酸对皮肤和衣服有很强的_______性
不慎将浓硫酸溅到皮肤或衣服上,应立即,然后涂上
在稀释浓硫酸时,一定要把_______沿,_______注入水中,并用_______不断搅拌
浓硫酸还具有很强的氧化性,它与较活泼的金属反应没有氢气生成
无吸水腐蚀浓硫酸器壁慢慢玻璃棒用大量水冲洗3%~5%NaHCO3的溶液放出大量的热浓盐酸是色液体,有气味,打开浓盐酸瓶盖,会见到,原因是什么
无刺激性白雾浓盐酸挥发出的氯化氢气体遇到空气中的水蒸气形成了盐酸小液滴浓盐酸挥发出了氯化氢气体使浓盐酸中的溶质质量变小
而浓硫酸则吸收了空气中的水蒸气,