国家药监局综合司关于印发医疗器械临床试验检查要点及判定原则的通知药监综械注〔2018〕45号2018年11月28日发布各省、自治区、直辖市食品药品监督管理局(药品监督管理局),核查中心:为加强医疗器械临床试验过程的监督管理,指导监管部门开展医疗器械临床试验监督检查工作,根据《医疗器械注册管理办法》和《医疗器械临床试验质量管理规范》要求,国家药品监督管理局组织制定了《医疗器械临床试验检查要点及判定原则》,现予以发布
国家药监局综合司2018年11月19日医疗器械临床试验检查要点及判定原则根据《医疗器械注册管理办法》和《医疗器械临床试验质量管理规范》等要求制定本检查要点及判定原则,用于指导医疗器械临床试验现场检查工作
一、检查要点序号现场检查要点检查内容1临床试验前准备1
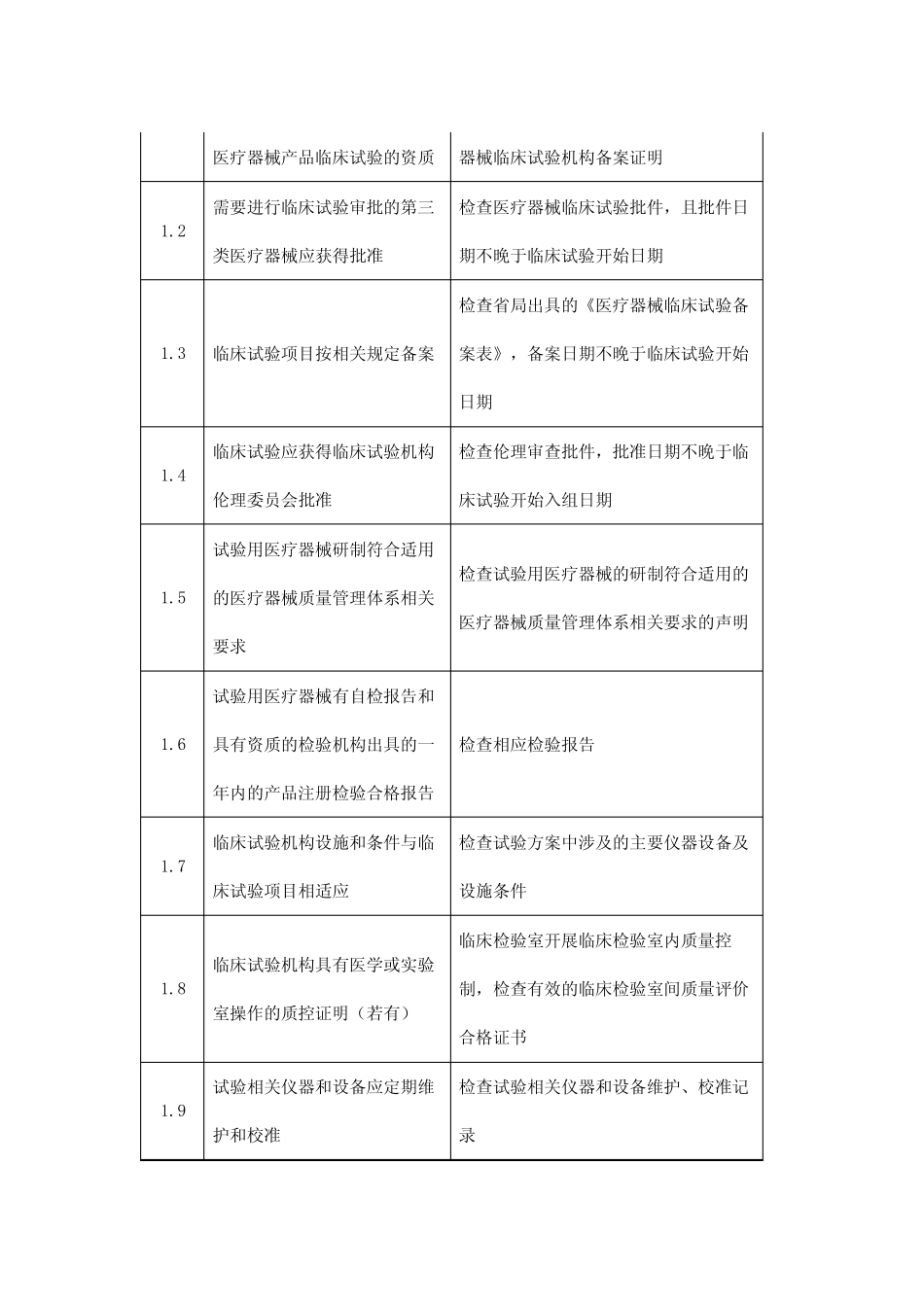
1临床试验机构应具有开展相关检查药物临床试验机构资格证明或医疗医疗器械产品临床试验的资质器械临床试验机构备案证明1
2需要进行临床试验审批的第三类医疗器械应获得批准检查医疗器械临床试验批件,且批件日期不晚于临床试验开始日期1
3临床试验项目按相关规定备案检查省局出具的《医疗器械临床试验备案表》,备案日期不晚于临床试验开始日期1
4临床试验应获得临床试验机构伦理委员会批准检查伦理审查批件,批准日期不晚于临床试验开始入组日期1
5试验用医疗器械研制符合适用的医疗器械质量管理体系相关要求检查试验用医疗器械的研制符合适用的医疗器械质量管理体系相关要求的声明1
6试验用医疗器械有自检报告和具有资质的检验机构出具的一年内的产品注册检验合格报告检查相应检验报告1
7临床试验机构设施和条件与临床试验项目相适应检查试验方案中涉及的主要仪器设备及设施条件1
8临床试验机构具有医学或实验室操作的质控证明(若有)临床检验室开展临床检验室内质量控制,检查有效的临床检验室间质量评价合格证书1
9试验相关仪器和设备应定期维护和校准检查试验