第四节化学反应中的能量变化【能力目标】1.使学生了解化学反应中的能量变化,并了解放热反应和吸热反应2.介绍燃料充分燃烧的条件,培养学生节约能源和环境保护的意识
3.使学生理解反应热的涵义
4.使学生掌握热化学方程式的书写方法和应用
5.使学生理解燃烧热并掌握有关燃烧热的计算
6.使学生理解中和热
【能力培养】1.化学反应中的能量变化(1)化学反应中的能量变化的本质原因物质变化的实质:旧化学键的断裂和新化学键的生成
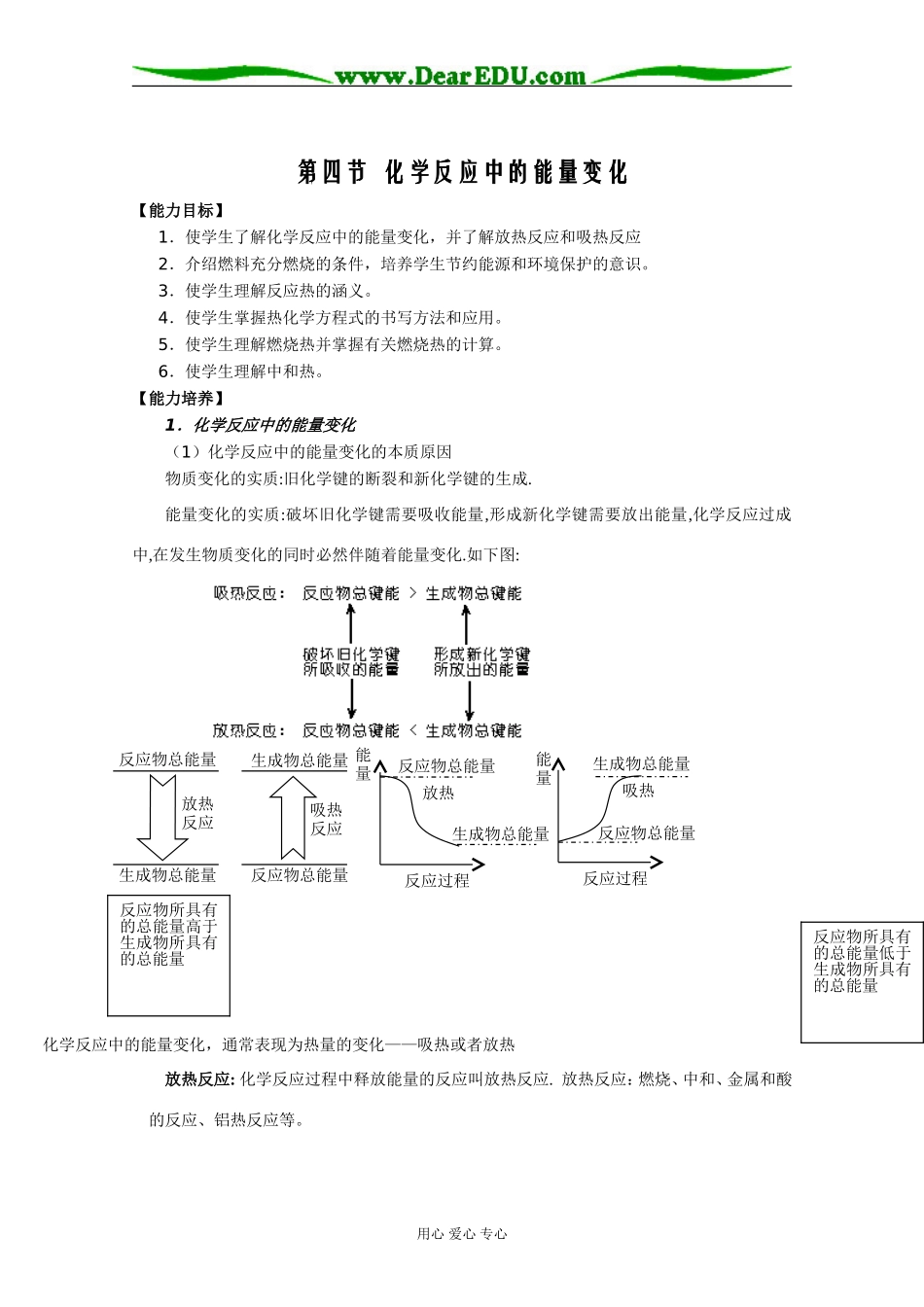
能量变化的实质:破坏旧化学键需要吸收能量,形成新化学键需要放出能量,化学反应过成中,在发生物质变化的同时必然伴随着能量变化
如下图:化学反应中的能量变化,通常表现为热量的变化——吸热或者放热放热反应:化学反应过程中释放能量的反应叫放热反应
放热反应:燃烧、中和、金属和酸的反应、铝热反应等
用心爱心专心反应物总能量反应物总能量反应物总能量生成物总能量生成物总能量生成物总能量放热反应吸热反应反应过程放热反应物总能量生成物总能量反应过程吸热能量能量反应物所具有的总能量低于生成物所具有的总能量反应物所具有的总能量高于生成物所具有的总能量吸热反应:化学反应过程中吸收能量的反应叫吸热反应
吸热反应:其特征是大多数反应过程需要持续加热,如CaCO3分解等大多数分解反应,H2和I2、S、P等不活泼的非金属化合,Ba(OH)2·8H2O和NH4Cl固体反应,CO2和C的反应
说明:吸热反应有的不需要加热如:Ba(OH)2·8H2O和NH4Cl固体反应,多数需要加热,放热反应有的开始时需要加热以使反应启动
即反应的吸、放热与反应条件无关
焓:用于表示物质所具有的能量的这一固有性质的物理量,叫做焓
化学反应的焓变△H:化学反应过程中反应物总能量与生成物总能量的变化叫做反应的焓变
热化学研究表明,对于在等压条件下进行的化学反应,如果反应中物质的能量变化全部转化为热能(同时可能伴随着反应体