2013高考化学二轮复习精品资料专题20物质结构与性质(教学案,教师版)3
了解简单配合物的成键情况
了解原子晶体的特征,能描述金刚石、二氧化硅等原子晶体的结构与性质的关系
理解金属键的含义,能用金属键理论解释金属的一些物理性质
了解杂化轨道理论及常见的杂化轨道类型(sp,sp2,sp3),能用价层电子对互斥理论或者杂化轨道理论推测常见的简单分子或者离子的空间结构
三、分子间作用力与物质的性质1
了解化学键和分子间作用力的区别
了解氢键的存在对物质性质的影响,能列举含有氢键的物质
了解分子晶体与原子晶体、离子晶体、金属晶体的结构微粒、微粒间作用力的区别
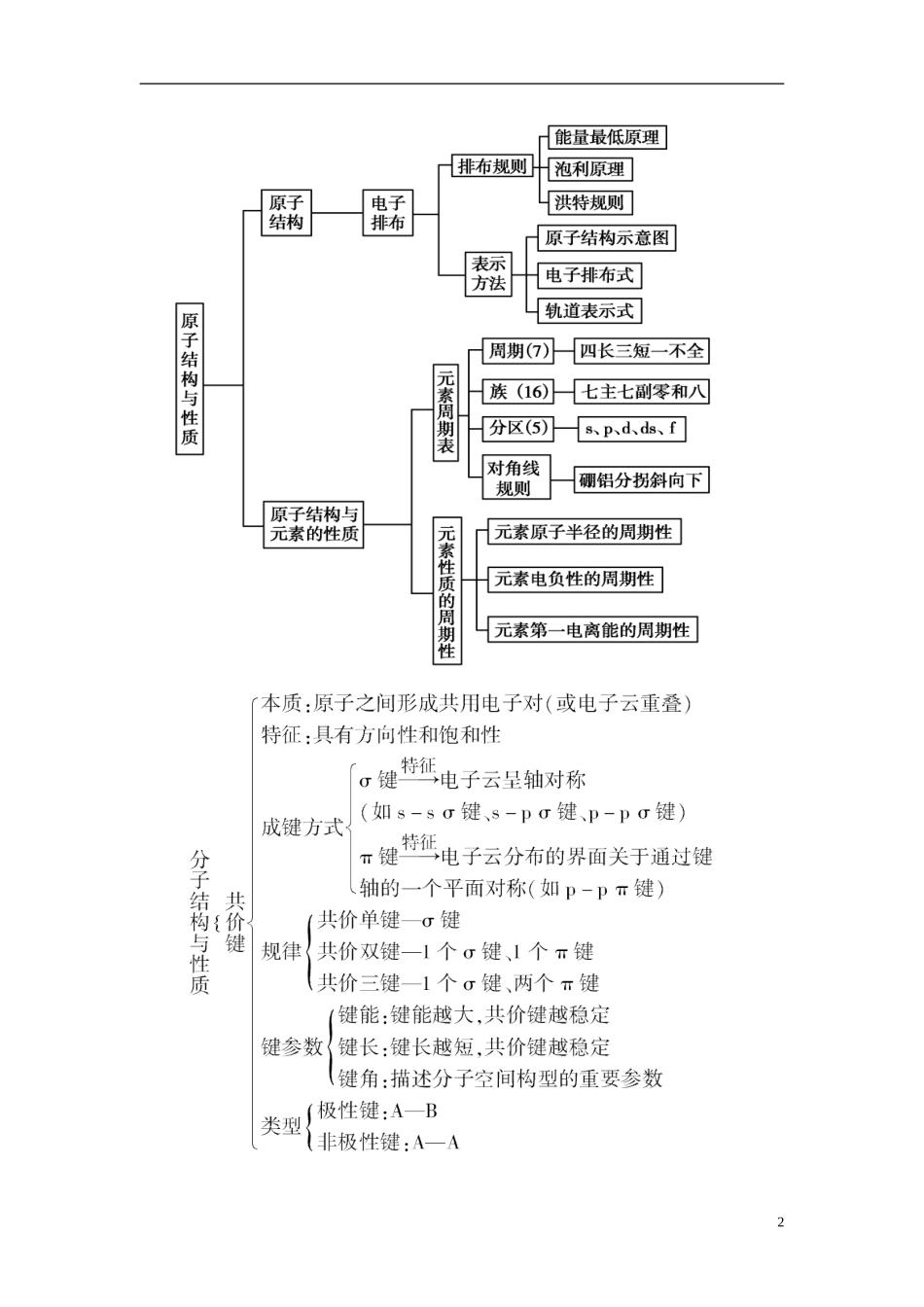
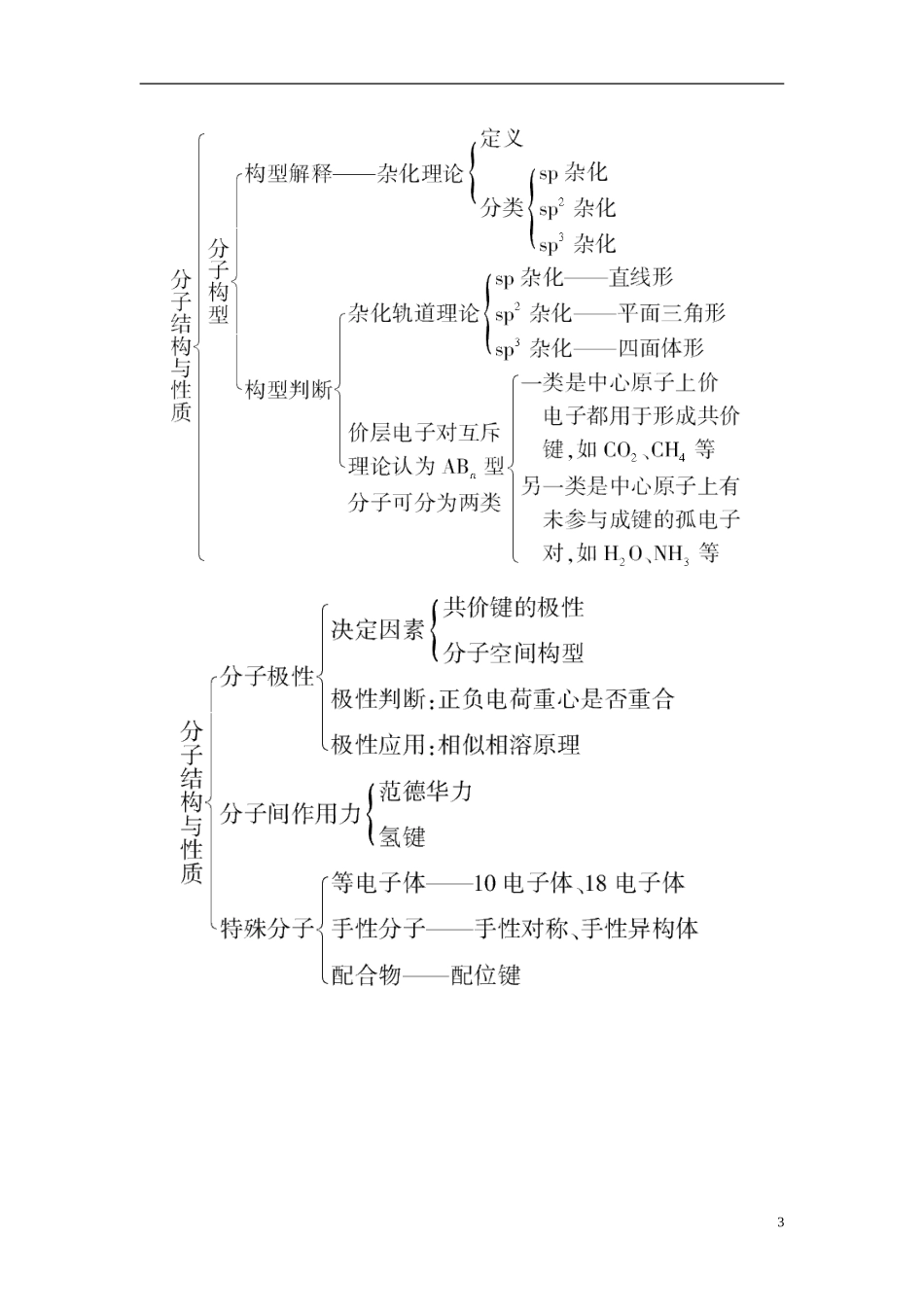
【知识网络】123【重点知识整合】一、原子结构与元素的性质1.基态原子的核外电子排布(1)排布规律①能量最低原理:基态原子核外电子先占有能量最低的原子轨道,如Ge:1s22s22p63s23p63d104s24p2
4②泡利原理:每个原子轨道上最多只容纳2个自旋状态不同的电子
③洪特规则:原子核外电子在能量相同的各轨道上排布时,电子尽可能分占不同的原子轨道,且自旋状态相同
注意:洪特通过分析光谱实验得出:能量相同的原子轨道在全充满(如d10)、半充满(如d5)和全空(如d0)时体系能量较低,原子较稳定
如Cr原子的电子排布式为[Ar]3d54s1;Cu原子的电子排布式为[Ar]3d104s1
(2)表示形式①电子排布式:用数字在能级符号右上角标明该能级上排布的电子数
如K:1s22s22p63s23p64s1或[Ar]4s1
②电子排布图:每个小方框代表一个原子轨道,每个箭头代表一个电子,如碳原子
2.电离能(1)同周期元素随着原子序数的递增,原子的第一电离能逐渐增大;但ⅡA族元素的第一电离能大于ⅢA族元素的第一电离能,ⅤA族元素的第一电离能大于ⅥA族元素的第一电离能
同主族元素,从上到下第一电离能逐渐减