第三节化学平衡(第二课时)【复习】化学平衡状态的定义:(化学反应的限度)化学平衡的特征:一定条件下,可逆反应里,正反应速率和逆反应速率相等,反应混合物中各组分的浓度保持不变的状态
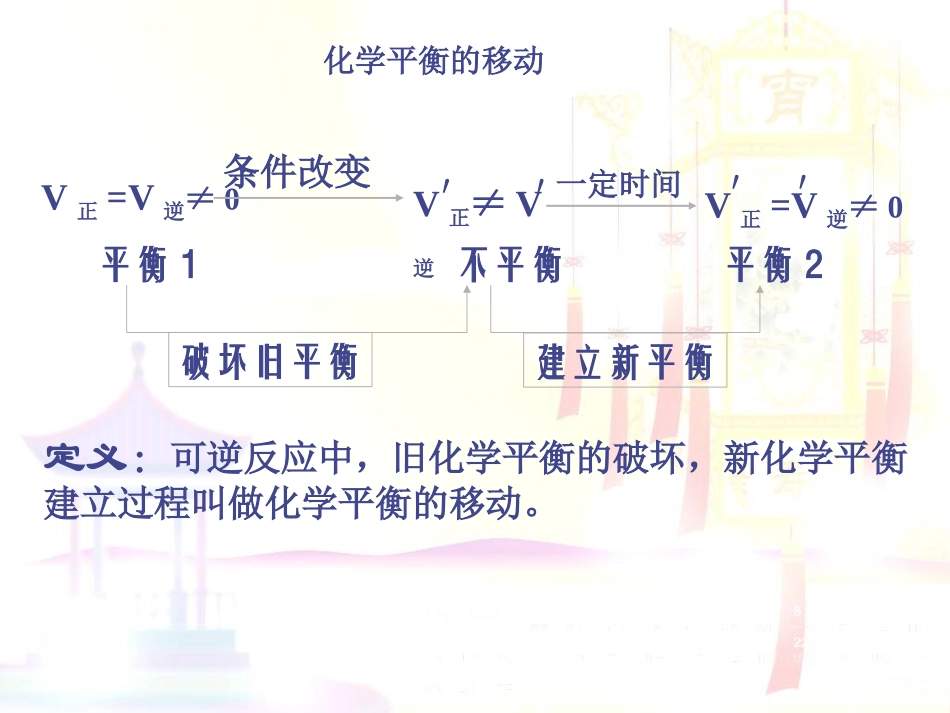
逆等动定变V正V逆V正=V逆vt0定义:可逆反应中,旧化学平衡的破坏,新化学平衡建立过程叫做化学平衡的移动
V正≠V逆V正=V逆≠0条件改变平衡1不平衡平衡2建立新平衡破坏旧平衡V正=V逆≠0′′一定时间化学平衡的移动′′浓度【回忆】影响化学反应速率的外界条件主要有哪些
化学反应速率温度压强催化剂【思考】如何通过改变条件来打破旧平衡
可通过改变影响反应速率的条件来打破原有平衡,建立新平衡
1、浓度对化学平衡的影响(P26)现象分析:Cr2O72-+H2O2CrO42-+2H+橙色黄色滴加3~10滴浓H2SO4滴加10~20滴6mol/LNaOHK2Cr2O7溶液增大c(H+)橙色加深C(Cr2O72-)增大平衡逆向移动平衡破坏减小c(H+)黄色加深C(CrO42-)增大平衡破坏平衡正向移动结论:增大生成物的浓度平衡向逆反应方向移动结论:减小生成物的浓度平衡向正反应方向移动溶液橙色加深溶液黄色加深现象及分析滴加饱和FeCl3溶液滴1mol/LKSCN溶液滴加NaOH溶液现象Fe3++3SCN-Fe(SCN)3增大c(Fe3+)增大c(SCN-)红色加深C[Fe(SCN)3)增大平衡破坏平衡正向移动结论:增大反应物的浓度平衡向正反应方向移动减小c(Fe3+)红色变浅C[Fe(SCN)3)减小平衡破坏平衡逆向移动结论:减小反应物的浓度平衡向逆反应方向移动Fe3++3OH-〓Fe(OH)3↓红色加深红色加深有红褐色沉淀生成,溶液红色变浅实验探究(P27实验2-6)浓度对化学平衡的影响在其他条件不变时,增大反应物浓度或减小生成物的浓度,化学平衡向正反应方向移动;减小反应物浓度或增大生成物的浓度化学平衡向逆