第二节 影响化学平衡的条件 第二课时(等效平衡问题) 1 、在一个恒容密闭容器里充入 1mol氮气和 3mol 氢气,使之在一定条件下发生反应达到平衡状态,发现容器内压强变为开始时的 0
( 1 )试求平衡时各组分的含量
( 2 )若开始往容器里加入 0
8mol 氮气, 2
4mol 的氢气和 0
4mol 的氨气,在相同情况下达到平衡后发现容器里的压强和第一种情况相同,请解释原因
等效平衡的问题: 在一定的条件下, 对于同一个可逆反应的同一个平衡状态(即任何相同组分的分数都相同),是可以由不同的途径达到的,我们把由不同途径到达的同一个平衡状态互称等效平衡
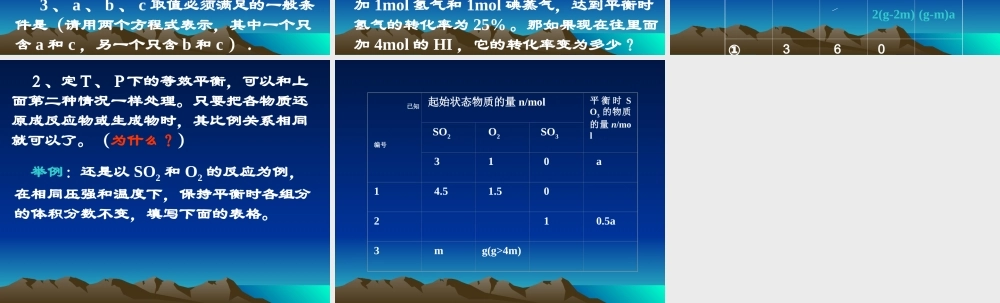
1 、定温、定容下的等效平衡: ① 对一般可逆反应来说,在 T 、V 一定的情况下,只要通过可逆反应的化学计量数比换算成左右两边同一物质的物质的量相同,则为等效平衡
举例:将 2molSO2 和 2molSO3气体混合于固定容积的密闭容器中,在一定条件下发生反应 2SO2 +O2 2 SO3 ,平衡时, SO3 为 nmol ,相同条件下,分别按下列配比放入起始物质,平衡时 SO3的量大于 n mol 的是( ) (A)2molSO2+1molO2 (B) 4molSO2+1molO2(C) 2 molSO2+1molO2+2molSO3(D) 3 molSO2+1molO2+1molSO3 练习题:在一定的温度下,把 2mol 的SO2 和 1mol 的氧气通入一密闭容器中,发生如下反应:2SO2+O2 2SO3 ,当此反应进行到一定程度时,反应混合物处于平衡状态
现在该容器的温度和体积不变,令 a,b,c 分别代表初始加入的 SO2 , O2 和 SO3 的物质的量( mol ),如果 a 、 b 、 c 取不同的值,必须满足一定的关系才可以保证在达到平衡时,反应混合物中三种气体的体积分数仍和上述