表面反应动力学1、假设气体A和B(压力分别为PA和PB)在催化剂上的吸附服从Langmuir吸附模型,反应生成气体M和N(压力分别为PM和PN),表面反应为控制步骤,其余均达平衡:A+BM+N*:为吸附位,KA=ka1/kd1,KB=ka2/kd2,KM=kd3/ka3,KN=kd4/ka4请推导反应速率方程
(共10分)反应速度:ka1*PA*θ=kd1*θAka2*PB*θ=kd2*θBka3*PM*θ=kd3*θMka4*PN*θ=kd4*θNθ+θA+θB+θM+θN=1,,2、简述固体催化剂上氧化还原反应的机理
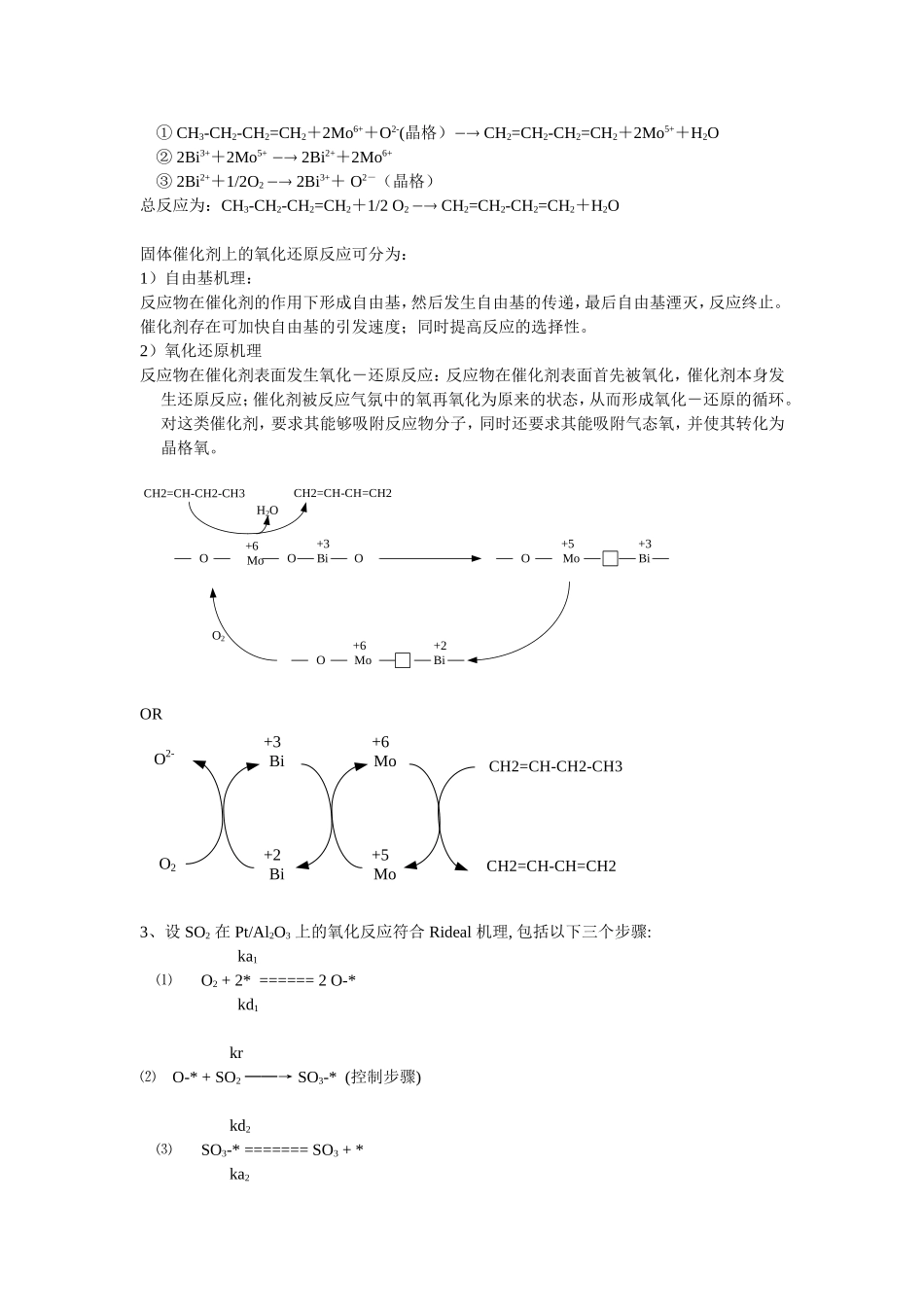
以1-丁烯氧化脱氢制丁二烯为例,画出其催化循环示意图
(共15分)所用催化剂为MoO3/Bi2O3混合氧化物,反应由下列各步组成:①CH3-CH2-CH2=CH2+2Mo6++O2-(晶格)CH2=CH2-CH2=CH2+2Mo5++H2O②2Bi3++2Mo5+2Bi2++2Mo6+③2Bi2++1/2O22Bi3++O2-(晶格)总反应为:CH3-CH2-CH2=CH2+1/2O2CH2=CH2-CH2=CH2+H2O固体催化剂上的氧化还原反应可分为:1)自由基机理:反应物在催化剂的作用下形成自由基,然后发生自由基的传递,最后自由基湮灭,反应终止
催化剂存在可加快自由基的引发速度;同时提高反应的选择性
2)氧化还原机理反应物在催化剂表面发生氧化-还原反应:反应物在催化剂表面首先被氧化,催化剂本身发生还原反应;催化剂被反应气氛中的氧再氧化为原来的状态,从而形成氧化-还原的循环
对这类催化剂,要求其能够吸附反应物分子,同时还要求其能吸附气态氧,并使其转化为晶格氧
OMoBiO+6+3CH2=CH-CH2-CH3CH2=CH-CH=CH2H2OOMoBi+5+3OMoBi+6+2OO2ORMoO2-+6Mo+5O2CH2=CH-CH=CH