+Zn(OH):OH
1©二-◎◎©展L-0®©©毗-Qe0商®◎◎J『第一章电化学腐蚀1、何为腐蚀原电池
(外电路短路,画图)腐蚀原电池:外电路短路原电池
2、何为次生腐蚀反应
举例说明(Fe)次生腐蚀反应:阳极、阴极腐蚀产物之间发生反应
如:Fe,Cu,3%NaCI溶液中;阳极:Fe-2e=Fe2+阴极:02+2H2O+4e=40H—次生腐蚀过程:Fe2++2OH-=Fe(0H)2Fe(0H)2沉积阳、极阴交界处形成致密膜起保护作用,若Fe(0H)2进一步反应:Fe(0H)2+02+2H2O=4Fe(OH)3,脱水成铁锈xFeO
yFe2O3
2H2O疏松不起保护作用
3、微电池的种类有哪些
定义:人眼不可辨,指阳极区和阴极区尺寸小,很难区分
(1)成分不均匀钢或铸铁中的Fe、Fe3C或石墨,Fe为阳极,Fe3C或石墨为阴极;(2)组织不均匀晶界与晶粒内部,一般晶界为阳极,晶粒内部为阴极;(3)物理状态不均匀应力大晶格畸变为阳极,应力小为阴极
4、双电层有哪几种
(1)金属+H2OMn+
ne+mH2O=Mn+
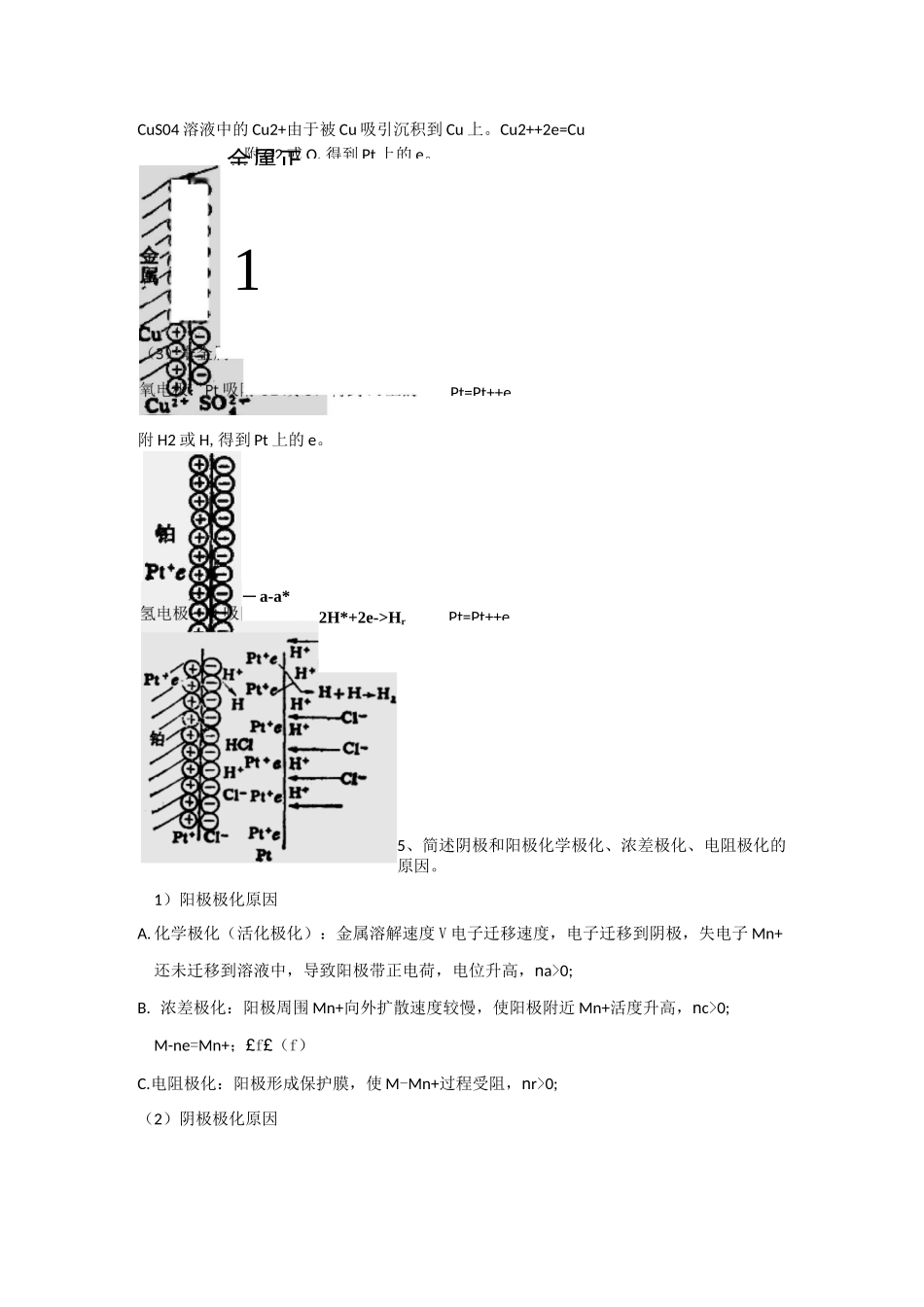
mH2O+ne2)金属+金属盐溶液Ze水平电IB属+电解质溶液Pt=Pt++eCuS04溶液中的Cu2+由于被Cu吸引沉积到Cu上
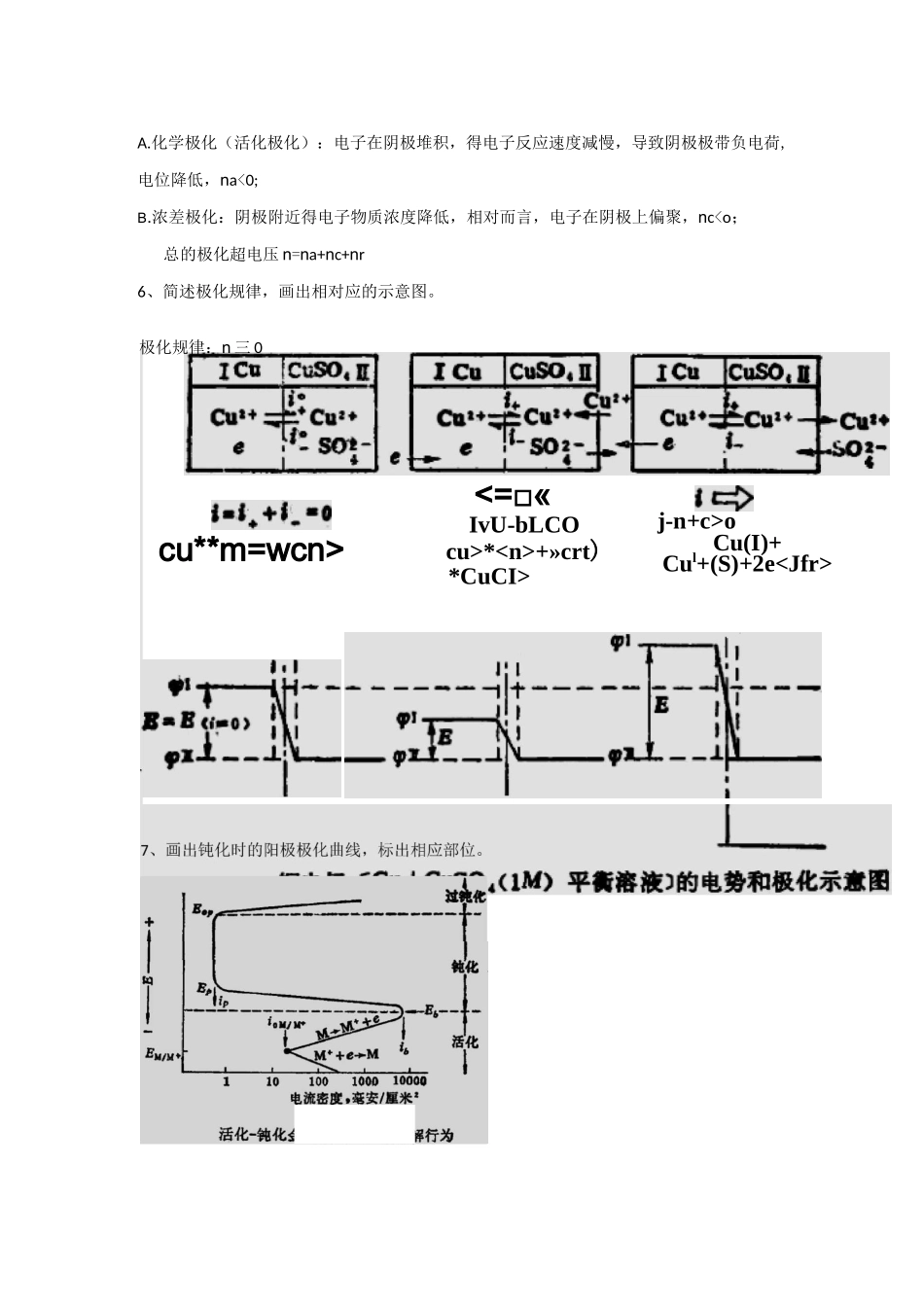
Cu2++2e=Cu附H2或H,得到Pt上的e
一a-a*2H*+2e->Hr5、简述阴极和阳极化学极化、浓差极化、电阻极化的原因
1)阳极极化原因A
化学极化(活化极化):金属溶解速度V电子迁移速度,电子迁移到阴极,失电子Mn+还未迁移到溶液中,导致阳极带正电荷,电位升高,na>0;B
浓差极化:阳极周围Mn+向外扩散速度较慢,使阳极附近Mn+活度升高,nc>0;M-ne=Mn+;£f£(f)C
电阻极化:阳极形成保护膜,使M-Mn+过程受阻,nr>0;(2)阴极极化原因金属正附O2或O,得到Pt上的e
Pt=Pt++e1A