实验十一电位——PHPHPHPH图的应用一、实验目的1
学会应用电位——PH图
1MNaHCO3(PH=8
4)溶液中的腐蚀情况,并对铁在此条件下进行阳极保护和阴极保护
二、基本原理电极电位的高低可以反映物质的氧化还原能力,从而判断电化学反应进行的可能性
大部分氧化还原反应和溶液的PH有关,将反应物质的电极电位与PH的关系绘成图,可直接从图上判断给定条件下反应进行的可能性或进行反应所必须的电位或PH条件,这种图称作电位——PH图或Pourbaix图
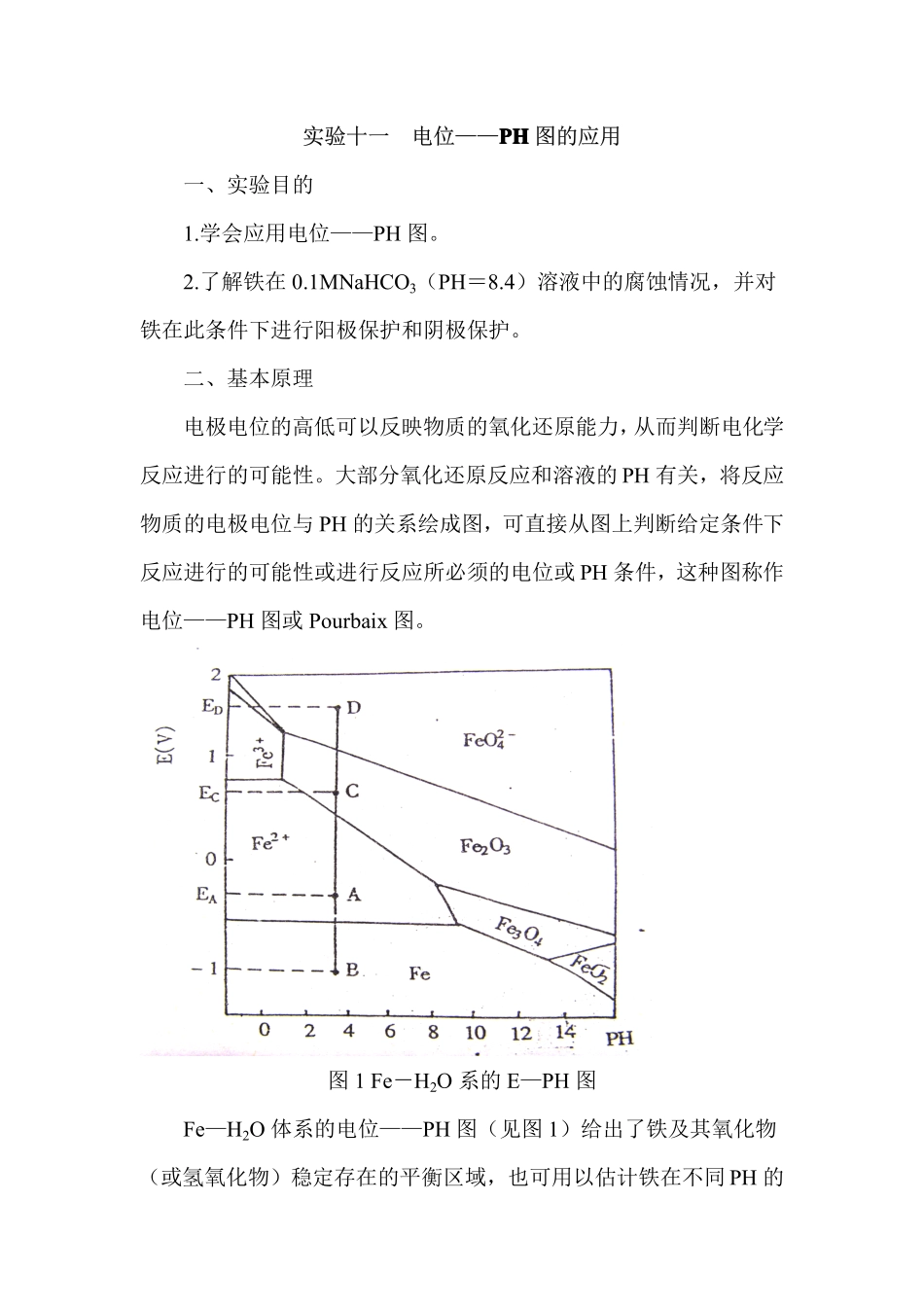
图1Fe-H2O系的E—PH图Fe—H2O体系的电位——PH图(见图1)给出了铁及其氧化物(或氢氧化物)稳定存在的平衡区域,也可用以估计铁在不同PH的水溶液中进行阳极保护和阴极保护的条件
例如图1中A点处于Fe2+稳定区,故金属铁将受到腐蚀而生Fe2+;但如果对它进行阳极极化,使其电位由EA提高到EC,因为图中C点处于Fe2O3的稳定区,所以在铁表面上生成一层Fe2O3膜,金属铁可由腐蚀状态进入钝化状态,使铁的腐蚀速度大大减小而受到保护
也可对金属铁进行阴极极化,即将电位由EA降低到EB
图1中B点处在铁的稳定区,所以金属铁将由腐蚀状态(A点)转变为热力学稳定状态,使铁的腐蚀停止而得到保护
如果金属铁处于图中D点的条件,该区域是FeO2-4的稳定区,这表明金属铁是处于过钝化状态
也可采用阴极极化使其电位由ED降低到EC,则金属铁从过钝化状态进入钝化状态而受到保护
三、实验仪器及用品直流稳压电源1台数字电压表1台毫安表1个电解池2个铂金电极2块饱和甘汞电极2个铁丝电极(φ=1
6mm,L=300mm)8根氮气1瓶氧气1瓶烧杯250~300mL(细长的)1个NaHCO3(0
1M,PH=8
4)2升H2SO42N四、实验步骤1
制作电极将L=40cm,φ=1
6mm的铁丝绕在φ=10mm的金属棒上,尾部留出4cm用于