1第三章水溶液中的离子平衡第二节水的电离和溶液的酸碱性第一课时2探究实验精确的纯水导电实验GG现象:指针摆动不亮结论:水是电解质极弱的HH22OO++HH22OHOH33OO++++OOHH--HH22OO++HH22OHOH33OO++++OOHH--HH22OHOH++++OHOH--HH22OHOH++++OHOH--能发生电离微弱的灵敏电流计灯泡3问题导学1
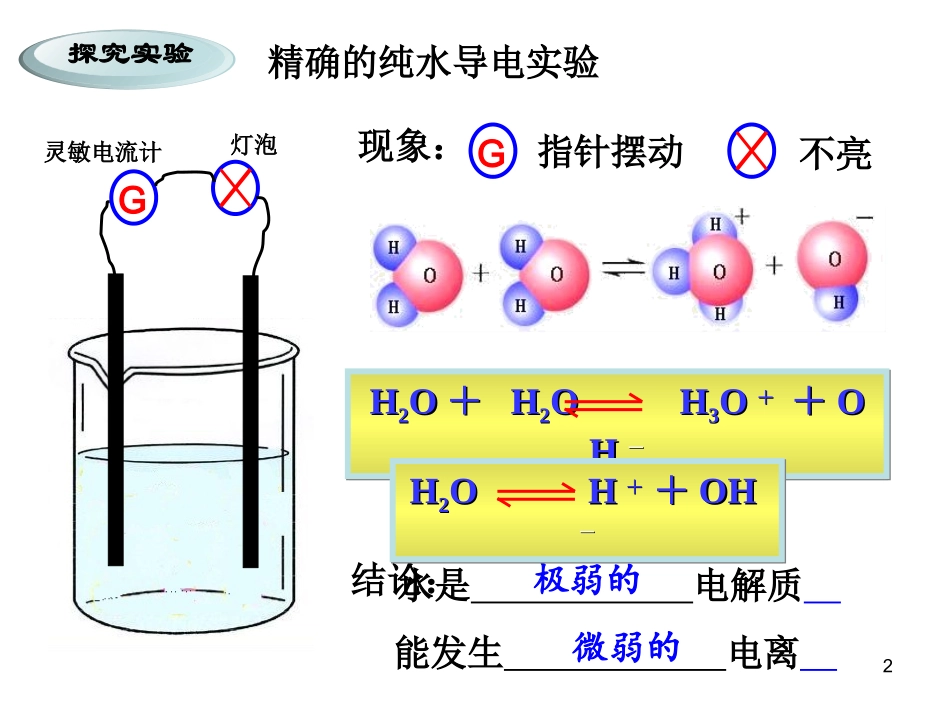
水的电离(1)如图所示用灵敏电流计测定纯水的导电性,请你认真观察、记录现象
(2)通过对上述现象的分析,谈一谈你对水电离与水的离子积的认识
学案P414答案:(1)灵敏电流计的指针发生微弱偏转
(2)①水是一种极微弱的电解质,只能微弱的电离,并存在着平衡
水的电离方程式:H2O+H2OH3O++OH-;简写为:H2OH++OH-
②从纯水的导电性实验测得,25℃时,1L纯水中只有1×10-7molH2O电离
所以c(H)+=c(OH-)=1×10-7mol·L-1,而1L水的物质的量为55
6mol,这与发生电离的水1×10-7mol相比,水的电离部分忽略不计
所以,电离前后,水的物质的量几乎不变,可以看作是一个常数,KW叫做水的离子积常数,简称水的离子积
KW=c(H+)·c(OH-)=1×10-7×1×10-7=1×10-14;水的离子积常数反映了一定温度下的水的H+浓度和OH-浓度之间的关系
5一、水的电离HH22OHOH++++OHOH--HH22OHOH++++OHOH--K电离=c(H+)·c(OH-)c(H2O)c(H+)·c(OH-)c(H2O)·K电离=室温下55
6molH2O中有1×10-7molH2O电离,平衡常数只和温度有关,因此c(H2O)·K电离可视为常数
Kw水的离子积Kw=室温下1×10-14注:c(H2O)=1L1000g18g·mol-161、分析表格中的数据,有何规律,并