官网:http://www
love中小学一对一课外辅导物质的结晶1
结晶:晶体从溶液中析出的过程
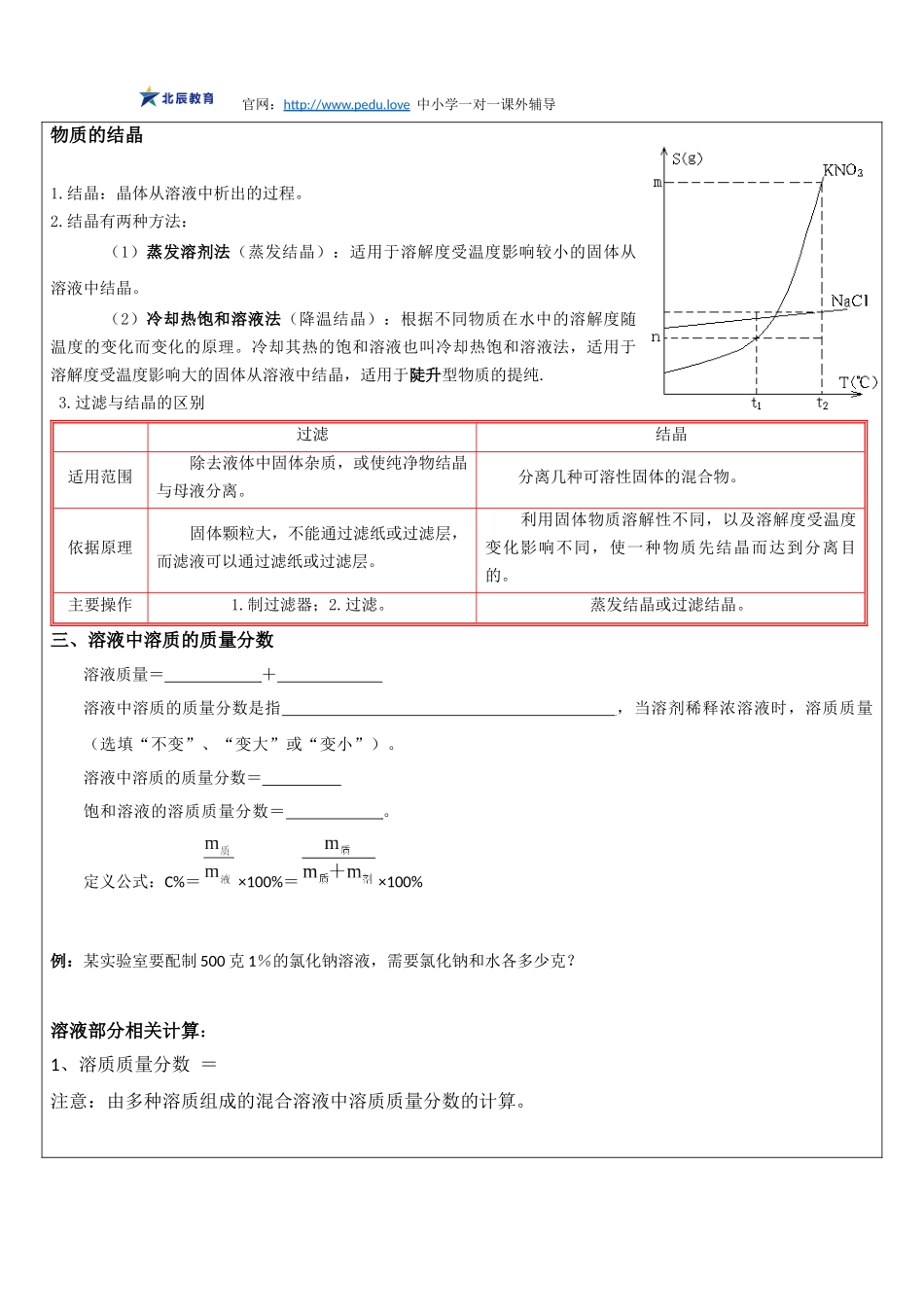
结晶有两种方法:(1)蒸发溶剂法(蒸发结晶):适用于溶解度受温度影响较小的固体从溶液中结晶
(2)冷却热饱和溶液法(降温结晶):根据不同物质在水中的溶解度随温度的变化而变化的原理
冷却其热的饱和溶液也叫冷却热饱和溶液法,适用于溶解度受温度影响大的固体从溶液中结晶,适用于陡升型物质的提纯
过滤与结晶的区别过滤结晶适用范围除去液体中固体杂质,或使纯净物结晶与母液分离
分离几种可溶性固体的混合物
依据原理固体颗粒大,不能通过滤纸或过滤层,而滤液可以通过滤纸或过滤层
利用固体物质溶解性不同,以及溶解度受温度变化影响不同,使一种物质先结晶而达到分离目的
制过滤器;2
蒸发结晶或过滤结晶
三、溶液中溶质的质量分数溶液质量=+溶液中溶质的质量分数是指,当溶剂稀释浓溶液时,溶质质量(选填“不变”、“变大”或“变小”)
溶液中溶质的质量分数=饱和溶液的溶质质量分数=
定义公式:C%=×100%=×100%例:某实验室要配制500克1%的氯化钠溶液,需要氯化钠和水各多少克
溶液部分相关计算:1、溶质质量分数=注意:由多种溶质组成的混合溶液中溶质质量分数的计算
官网:http://www
love中小学一对一课外辅导2、溶液质量与体积之间的换算:溶液质量(克)=溶液体积(毫升)×溶液密度(克/毫升)3、溶液的稀释:m浓溶液×a%=m稀溶液×b%(a>b)其中:m稀溶液=m浓溶液+m水若用溶质质量分数不同(a%、b%)的溶液A、B,配制中间溶质质量分数的溶液(c%),则:mA×a%+mB×b%=(mA+mB)×c%7、溶解度、溶质质量分数计算公式,关系:饱和溶液中溶质质量分数=×100%8、饱和溶液与不饱和溶液的相互转化一般:(特例:熟石灰)①降温②加溶